中国科学院上海高等研究院研究员王丽华带领团队在光控DNA微纳制造方面取得进展,相关研究成果以Remote Photothermal Control of DNA Origami Assembly in Cellular Environments为题,发表在Nano Letters上。
DNA折纸(DNA origami)结构是由一条数千碱基长的噬菌体DNA在上百条短单链DNA辅助下折叠形成的纳米结构,具有可程序化定制的形貌以及近原子级的结构精度,近年来在仿生纳米机器人、生物智能诊疗等领域展现出应用潜力。因此,在生理环境下原位合成DNA折纸结构成为迫切需求。然而,DNA折纸合成需要打开DNA分子预先形成的错误结构,才能保证正确的DNA折叠过程。传统DNA折纸合成技术往往依赖全局的、接触式的加热-退火的方式来完成这一过程,难以实现远程可控的生理环境原位合成。
科研人员受近红外光热治疗的启发,利用硫化铜纳米粒子作为光热转换材料,用近红外光(NIR)照射在合成溶液中产生光热效应,以打开DNA分子的二级结构,促使其在自然冷却下形成正确的折纸结构(图1)。该方法的优势在于DNA折纸合成速度快,仅需8分钟即可达到大于80%的产率,而传统的合成方法需要数小时。此外,该方法可在活细胞培养环境中实现具有时空可控性的DNA折纸原位合成(图2)。
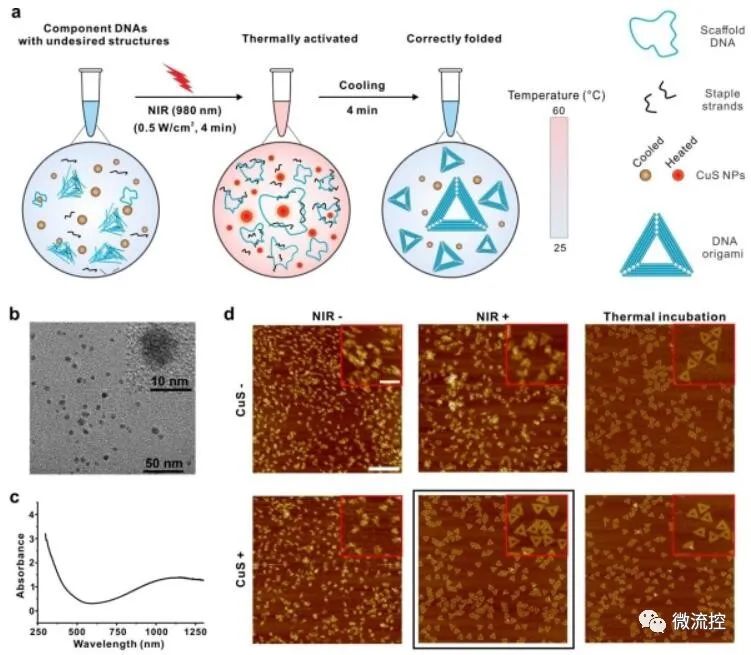
图1 红外光热效应远程、时空控制的DNA Origami的合成。(a)合成的示意图。(b)CuS NPs的透射电镜图。(c)硫化铜的紫外-可见光-红外吸收曲线。(d)各种合成产物的原子力显微镜图。
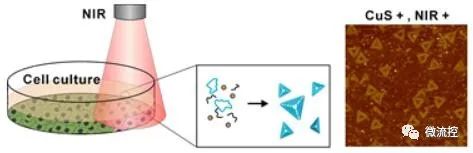
图2 细胞环境中DNA折纸的远程、可控的原位合成。
由于近红外光热系统具有深层组织穿透能力,并已广泛应用于生物系统,因此该工作有望实现光控的DNA纳米装置活体内原位组装与重构,使其在体内的时空分布和功能得到响应性调控,具有应用于生物计算和活体智能诊疗的前景。
研究工作得到国家重点研发计划、国家自然科学基金等的资助。
论文链接:
https://pubs.acs.org/doi/10.1021/acs.nanolett.1c01821
