全固态电池(ASSBs)由于其高安全性、高能量密度等优势受到广泛关注。卤化物电解质因为具有高离子电导率(≥10-4 S/cm)、高氧化电位(≥4.2 Vvs. Li/Li+)和良好机械柔韧性,已成为固态电池电解质的重要研究方向。然而当采用NCM层状氧化物作为正极材料时,其与卤化物电解质间的界面副反应会导致容量持续衰减。此外,商用氧化物正极材料具有较大的颗粒硬度,以及在脱锂/嵌锂过程中存在剧烈的晶格体积变化,容易导致充放电过程中正极内部应力分布不均,引发颗粒间固-固接触失效及颗粒内部裂纹裂隙,加速电极结构退化及电池失效。因此,为满足新能源汽车和储能系统对长寿命电池的需求,开发新型正极材料并优化正极/电解质界面稳定性,已成为实现高性能卤化物基全固态电池的关键技术挑战。近日,中山大学章志珍、司锐以及中国科学院物理研究所胡勇胜等人报告了一种新型卤化物正极材料Li2-2xFe1+xCl4(0≤x≤1/3),并对其脱嵌锂过程进行了深入的研究。得益于Li2FeCl4材料与卤化物电解质优异的化学及电化学稳定性,以及在脱嵌锂过程中的极小的晶格体积变化(3.2%),Li2FeCl4全固态电池表现出优异的倍率性能和循环稳定性。Li2FeCl4全固态电池在1C倍率下循环1000次后,容量保持率高达94.6%。且在10C的大倍率下,Li2FeCl4全固态电池循环5000次后仍可保持90.5 mAh g-1的可逆容量,容量保持率为85.1%。此外,通过调整Li:Fe比值,制备出的Li4/3Fe4/3Cl4表现出155.2 mAh g-1的高可逆容量,接近LiFePO4正极材料的实际可逆容量。这项研究强调了卤化物正极材料在卤化物电解质基全固态电池中的优势,有望启发更多高性能卤化物基全固态电池的研究。该文章发表在国际顶级期刊ACS Energy Letters上。博士生彭德招、李瑞为本文第一作者。在新型锂离子正极材料的开发中,材料体系的选择需兼顾离子传输动力学、脱嵌锂过程中的结构稳定性和与电解质的界面兼容性等核心要素。本研究选用铁基氯化物Li2-2xFe2+xCl4(0 ≤ x ≤ 1/3)作为研究对象,主要基于以下考量:首先,现有研究表明卤化物电解质体系具有优异的离子电导率。选择与卤化物电解质具有相似晶体结构的卤化物作为正极材料,其具有潜在的快速锂离子传输能力。其次,Fe2+/Fe3+氧化还原对在氯化物中展现出3.6-3.8 V(vs. Li+/Li)的稳定工作电位区间,既保证了足够高的能量密度,又避免了传统NCM材料在高电位下引发的电解质分解问题。更重要的是,采用与固态电解质元素组成和结构相似的卤化物正极材料,可从根本上解决界面相容性问题。这种材料设计策略能够有效抑制界面副反应,为构建高性能卤化物基全固态电池体系提供了创新解决方案。Li2-2xFe1+xCl4 (0 ≤ x ≤ 1/3)材料物相及离子迁移方式分析
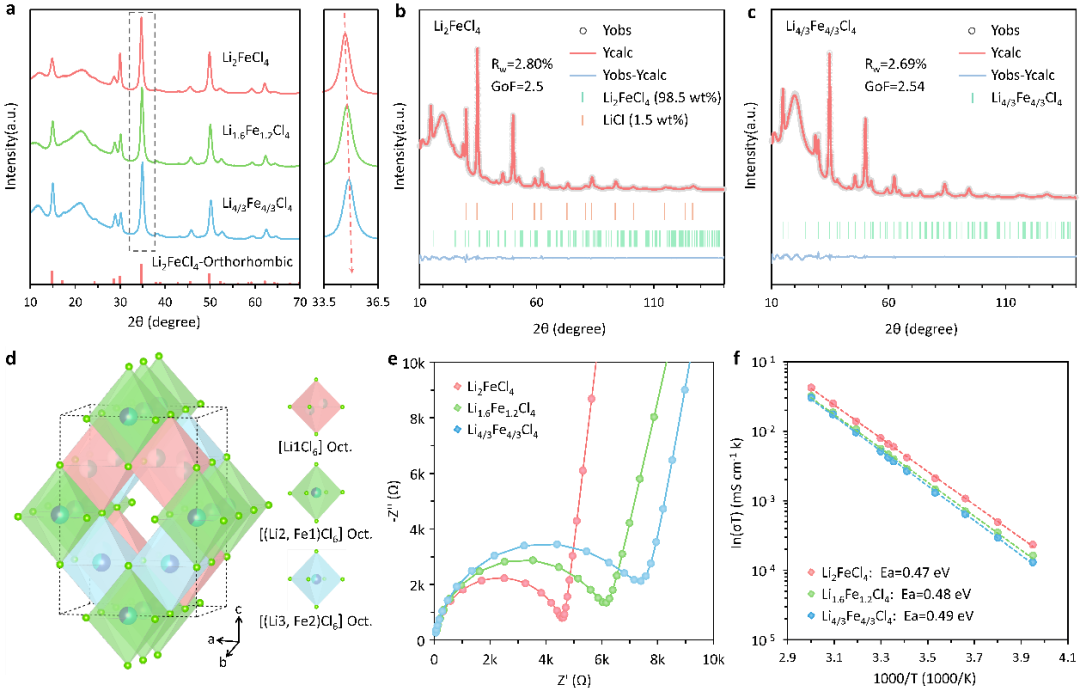
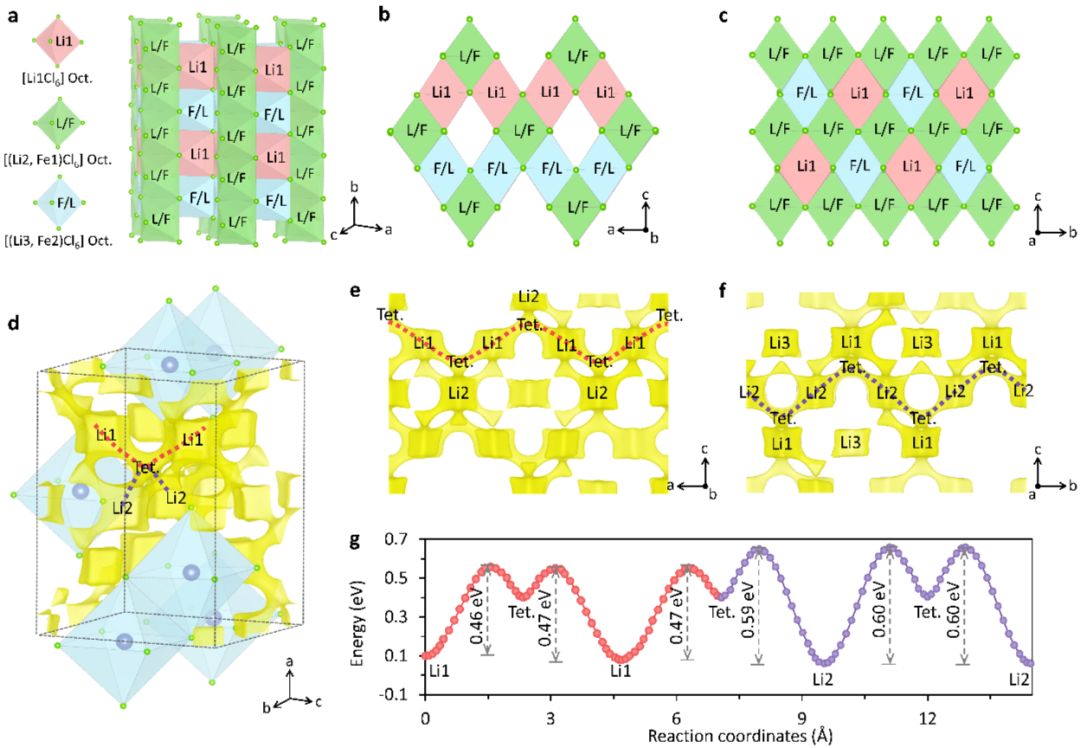
Li2-2xFe1+xCl4 (0 ≤ x ≤ 1/3)材料均形成了正交系相结构,且随着x值增大,晶胞延c轴方向缩小(a、b轴变化较小)。XRD的Rietveld精修表明在Li2FeCl4晶体中,Li+占据了三个不同的晶格位点:8i(Li1)、4b(Li2)和4d(Li3),对应的占据比例分别为0.50、0.725和0.275,而Fe2+则与Li+共享4b(Fe1)和4d(Fe2)位点。图1 (a) Li2-2xFe1+xCl4(x = 0, 0.2和1/3)的X射线衍射图;(b) Li2FeCl4的X射线衍射图及Rietveld精修。(c) Li4/3Fe4/3Cl4的X射线衍射图及Rietveld精修;(d) Li2FeCl4的晶体结构;(e) 室温下Li2-2xFe1+xCl4(x = 0, 0.2和1/3)的交流阻抗谱图。(f) -20 oC ~60 oC下Li2-2xFe1+xCl4(x = 0, 0.2和1/3)的阿伦尼乌兹曲线。Li2FeCl4的晶格排列方式如下:[(Li2, Fe1)Cl6]八面体沿b轴共边连接,[(Li3, Fe2)Cl6]八面体和[Li1Cl6]八面体在a轴共边排列。基于键价位能(BVSE)计算,Li+在三维扩散网络中的迁移路径呈现各向异性:在ac平面,Li+通过弯曲的[Li1Cl6]八面体-四面体间隙-[Li1Cl6]八面体在共边连接的[Li1Cl6]八面体之间迁移,迁移能垒为0.47 eV;在bc平面(图2f),Li+通过[(Li2, Fe1)Cl6]八面体-四面体间隙-[(Li2, Fe1)Cl6]八面体在共边连接的[(Li2, Fe1)Cl6]八面体之间迁移,迁移能垒为0.60 eV。图2 (a) Li2FeCl4的2×2×1超级晶胞,粉色八面体代表[LiCl6]八面体,绿色八面体代表[(Li2, Fe1)Cl6]八面体,蓝色八面体代表[(Li3, Fe2)Cl6]八面体;(b) Li2FeCl4的2×2×1超级晶胞沿(010)方向的二维视图,(c) BVSE结果中Li2FeCl4的2×2×1超级晶胞沿(100)方向的二维视图;(d) BVSE结果中Li2FeCl4的1×1×1晶胞的Li+迁移路径;(e) 位能等值面在ac平面的二维视图,用红色曲线表示Li+离子的迁移路径;(f) 位能等值面在bc平面的二维视图,用紫色曲线表示Li+离子的迁移路径;(g) Li2FeCl4的离子跃迁势垒,红色和蓝色曲线分别代表e和f中Li+离子的迁移路径势垒。2 Li2FeCl4材料电化学性能及脱嵌锂机制分析
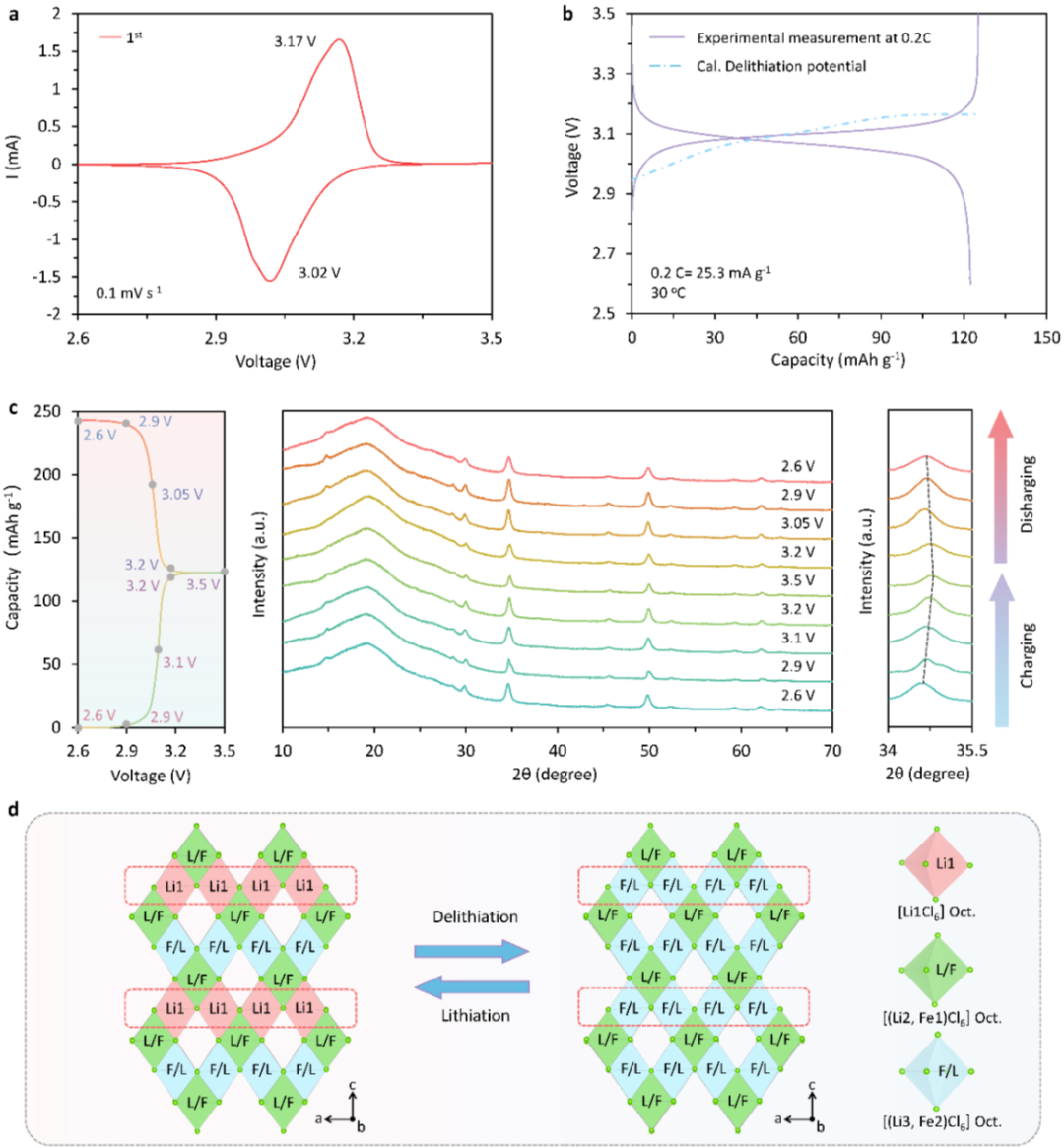
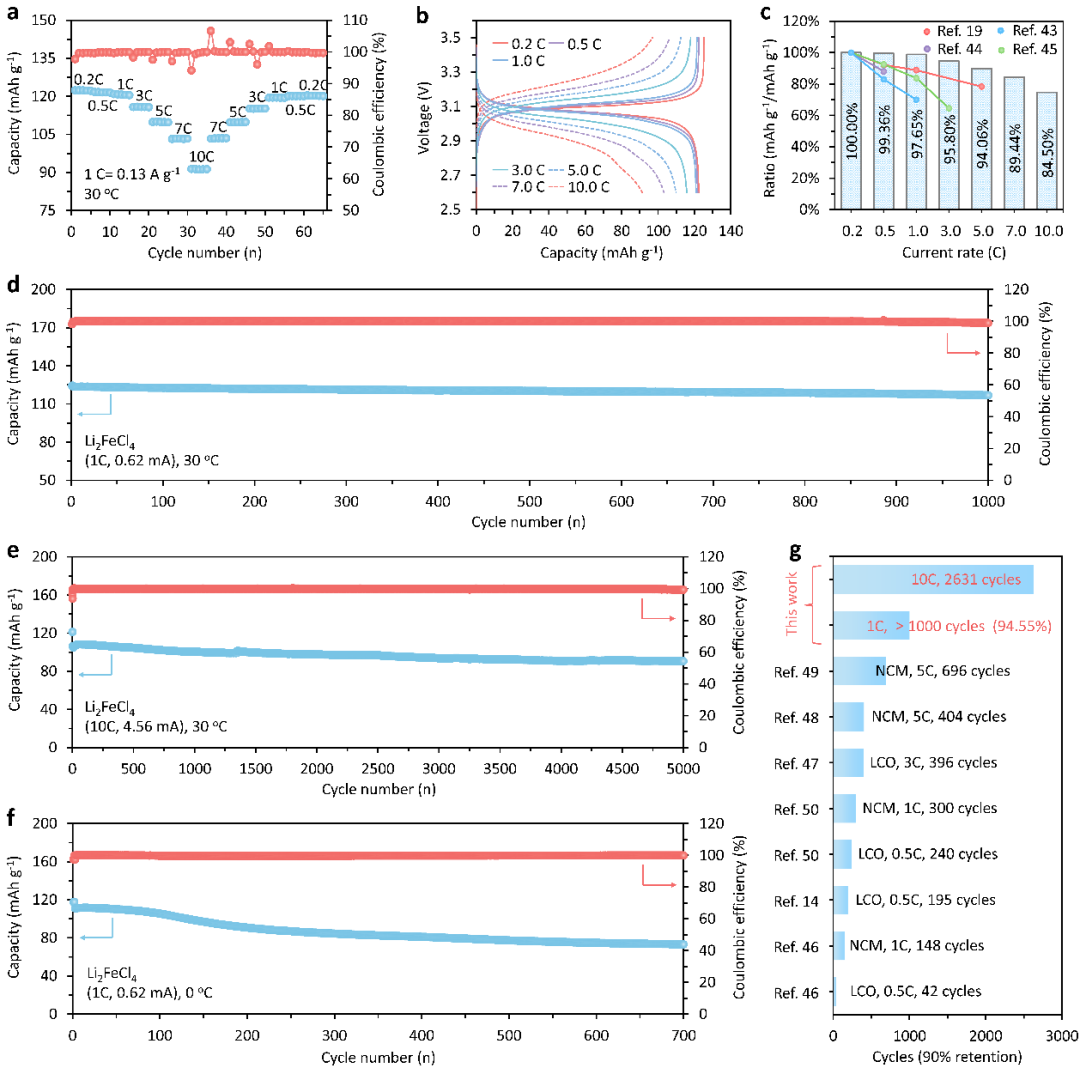
Li2FeCl4全固态电池在3.17/3.02 V(vs. Li+/Li-In))处表现出Fe3+/Fe2+氧化还原反应。0.2C倍率下Li2FeCl4全固态电池首周充电比容量达125.2 mAh g-1,接近其理论比容量(126.7 mAh g-1),且放电比容量为122.3 mAh g-1,首圈库伦效率为97.8%。非原位XRD表明Li2FeCl4的(220)晶面衍射峰随脱锂过程向高角度偏移(从34.65o到34.75o),表明由于Li+的脱出而导致晶格收缩。在随后的放电过程中,(220)晶面对应的衍射峰逐渐向低角度偏移,直至回到其原始位置,表明Li2FeCl4的锂脱嵌过程具有高度可逆性。XRD图谱显示整个充放电过程中未出现新的衍射峰,表明Li2FeCl4的脱嵌锂过程为固溶行为。DFT计算表明脱锂过程伴随3.2%的体积收缩,显著低于NCM(7.3%)和LiFePO4(6.8%),有利于实现优异的循环稳定性。为了分析Li2FeCl4在锂脱嵌过程中锂位点占据率的变化规律,DFT计算表明从Li2或Li3位点脱出Li+的平均能量比从Li1位点的能垒高约330 mV,导致Li1位点上的Li+优先脱出。因此,在充电过程中,Li1位点上的Li+依次从八面体位点脱出,直到从Li2FeCl4中Li1位点所有锂离子均被脱出。图3 (a) Li2FeCl4全固态电池的CV曲线,电压范围为2.6~3.5 V (vs. Li/Li-In);(b) 0.2C下Li2FeCl4全固态电池的首圈充放电曲线(紫色),蓝色虚线为DFT计算的Li2FeCl4的脱锂电位;(c) Li2FeCl4正极的非原位XRD曲线,以及(220)晶面所对应的衍射角度随充放电状态改变的变化规律;(d) Li2FeCl4在脱嵌锂过程中晶体结构变化示意图。在1C的电流密度下,Li2FeCl4全固态电池首圈可逆容量为120.9 mAh g-1,与0.2C下的可逆容量相比没有明显下降。当电流密度提升至5C和10C时,电池可逆容量分别为109.9 mAh g-1和91.4 mAh g-1。相比于0.2C下的可逆容量,5C和10C下的容量保持率分别为89.9%和74.8%,远高于氧化物正极材料在相同条件下的容量保持率。此外,Li2FeCl4全固态电池在1C下循环1000次,容量保持率为94.6%;并以10C的大电流密度循环5000次后,容量保持率为容量保持率为85.1%,平均每圈容量衰减0.003%。图4 (a) 室温下Li2FeCl4全固态电池的倍率性能;(b) Li2FeCl4全固态电池在不同倍率的充放电曲线;(c) Li2FeCl4全固态电池在不同倍率下放电容量与在0.2C放电容量的比值,以及文献中报道的其他全固态电池的数值;(d) 在室温、1C下Li2FeCl4全固态电池的循环性能;(e) 在室温、10C下Li2FeCl4全固态电池的循环性能;(f) 在0 oC、1C下Li2FeCl4全固态电池的循环性能;(g) 本研究中Li2FeCl4全固态电池与文献报道的其他全固态电池循环稳定性的比较,横坐标为电池放电容量衰减至90%时的循环圈数。3 Li4/3Fe4/3Cl4材料电化学性能及脱嵌锂机制分析
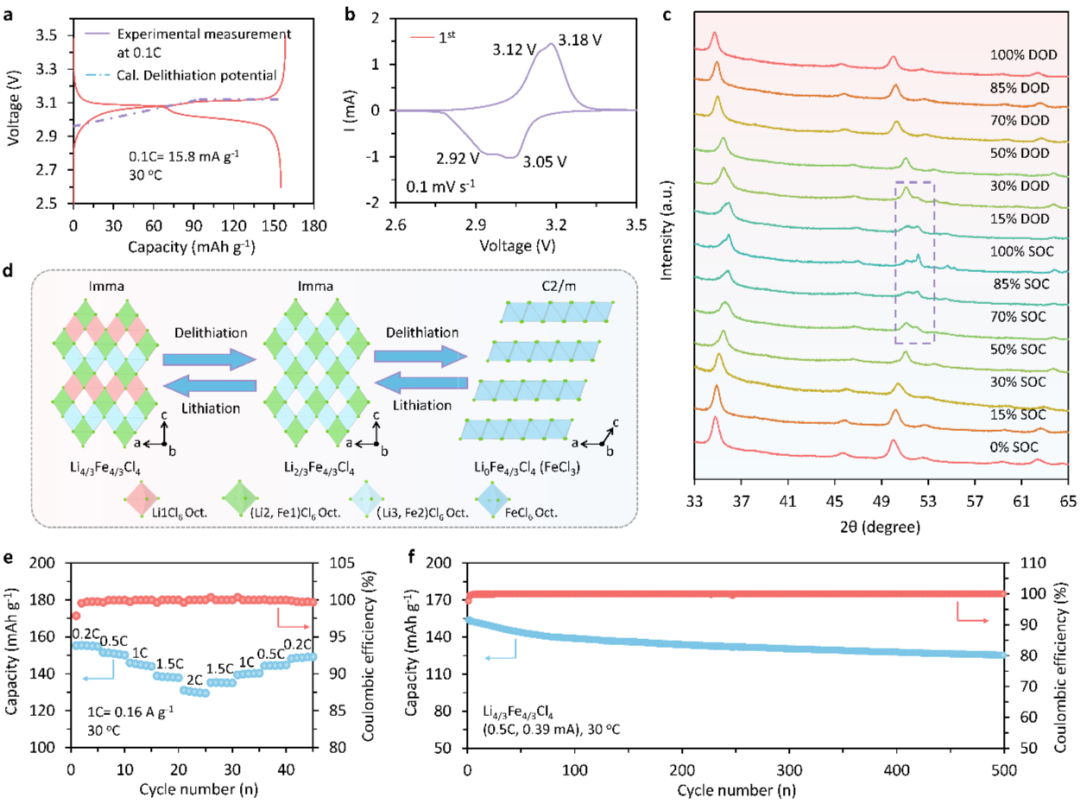
当x=1/3时(Li2-2xFe1+xCl4,0 ≤ x ≤ 1/3),Li4/3Fe4/3Cl4具有最高的理论比容量158.4 mAh g-1(对应于每个分子的4/3个电子氧化还原反应)。组装的全固态电池的首圈可逆容量为154.2 mAh g-1,接近LiFePO4正极材料的实际可逆容量。与Li2FeCl4不同,Li4/3Fe4/3Cl4全固态电池的充放电曲线表现出两段电压平台,并在CV测试中表现出两对氧化还原峰(3.05 V/3.18 V和2.92 V/3.12 V)。非原位XRD测试表明,当电池电压处于第一个平台时,正极材料XRD衍射峰逐渐向高角度偏移,但没有新的衍射峰出现,因此该阶段锂脱出过程为固溶行为。当电池进一步充电至第二个电压平台,在52o出现一个新的衍射峰,同时50o衍射峰逐渐减弱,表明该过程为两相共存的相转变过程。完全脱锂后的Li0Fe4/3Cl4材料(化学计量比相当于FeCl3)为C2/m结构。在1C及2C电流密度下,Li4/3Fe4/3Cl4全固态电池的放电比容量分别为146.0 mAh/g和131.1 mAh/g。另外,电池在0.5C电流密度下循环500圈后,容量保持率为86.0%。相比于Li2FeCl4材料,Li4/3Fe4/3Cl4容量衰减速度明显加快,这主要归因于相转变过程大的体积变化导致正极内部产生大量裂隙。图5 (a) 0.1C下Li4/3Fe4/3Cl4全固态电池的首圈充放电曲线;(b) Li4/3Fe4/3Cl4全固态电池的CV曲线,电压范围为2.6~3.5 V (vs. Li/Li-In);(c) 不同充放电状态下Li4/3Fe4/3Cl4全固态电池的正极XRD图谱;(d) Li4/3Fe4/3Cl4在脱嵌锂过程中晶体结构变化示意图;(e) 室温下Li4/3Fe4/3Cl4全固态电池的倍率性能;(f) 在室温、0.5C下Li4/3Fe4/3Cl4全固态电池的循环性能。本研究成功开发新型铁基卤化物正极材料Li2-2xFe1+xCl4(0 ≤ x ≤ 1/3)。其中,基于Li2FeCl4材料构建的全固态电池展现出优异倍率性能和长循环寿命。针对高比容量材料Li4/3Fe4/3Cl4,揭示了其两阶段(固溶-相变)脱锂反应机制及其容量衰减的内在原因。该工作不仅构建了低成本、高稳定性的铁基氯化物正极体系,有效缓解了传统氧化物正极的界面稳定性问题,更为多价金属氯化物电极设计提供了重要的Li+脱嵌锂位点理论指导。Dezhao Peng, Rui Li, Kaiqi Xu, Rui Si*, Zhizhen Zhang*, Yong-Sheng Hu*, A Low-Strain Lithium Cathode Material Li2-2xFe1+xCl4 for Halide-Based All-Solid-State Batterie. ACS Energy Lett. 2024.https://pubs.acs.org/doi/full/10.1021/acsenergylett.4c03147
锂电联盟会长向各大团队诚心约稿,课题组最新成果、方向总结、推广等皆可投稿,请联系:邮箱libatteryalliance@163.com或微信Ydnxke。
工艺,研发,机理和专利!软包电池方向重磅汇总资料分享!
搞懂锂电池阻抗谱(EIS)不容易,这篇综述值得一看!锂电池循环寿命研究汇总(附60份精品资料免费下载)