心型脂肪酸结合蛋白(H-FABP)是一种主要存在于心脏、骨骼肌和肾脏中的小分子蛋白,参与脂肪酸的转运和代谢,在心脏能量代谢中起关键作用。H-FABP可作为心脏损伤的早期生物标志物,广泛用于急性心肌梗死和心衰等心脏疾病的诊断。因此,建立高效的H-FABP检测手段,对心脏疾病的早期预警和精准诊断,以及保障公众生命健康安全具有重要意义。然而,传统的单一模式传感器容易受到外界因素的干扰,从而影响结果的准确性。纳米酶作为天然酶的替代物,因其独特的物理化学性质,展现出广泛的应用潜力。与传统天然酶相比,纳米酶具备较高的稳定性和耐高温、耐酸碱性,能在多种反应条件下保持活性。
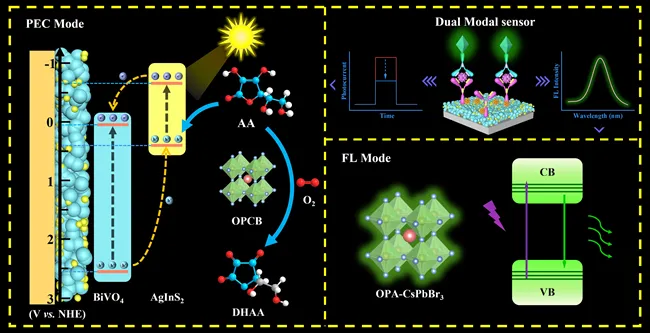
济南大学魏琴团队和山东大学蔡彬团队合作开发了一种基于两亲性聚合物修饰的钙钛矿纳米酶的光电化学(PEC)/荧光(FL)双模式微流控传感平台。利用CsPbBr3纳米酶的类抗坏血酸氧化酶活性及荧光活性,实现对H-FABP的双模式检测。两种方法的检出限分别是36 fg/mL(PEC)和0.32 pg/mL(FL)。该工作拓展了钙钛矿纳米酶在生物传感领域的应用。
该研究以辛胺修饰的聚丙烯酸和油胺作为配体合成了具有良好水稳定性的CsPbBr3纳米酶(OPCB)。在微流控芯片中,纳米酶的酶活性被充分发挥,实现了对电子供体抗坏血酸的催化氧化,猝灭了PEC信号。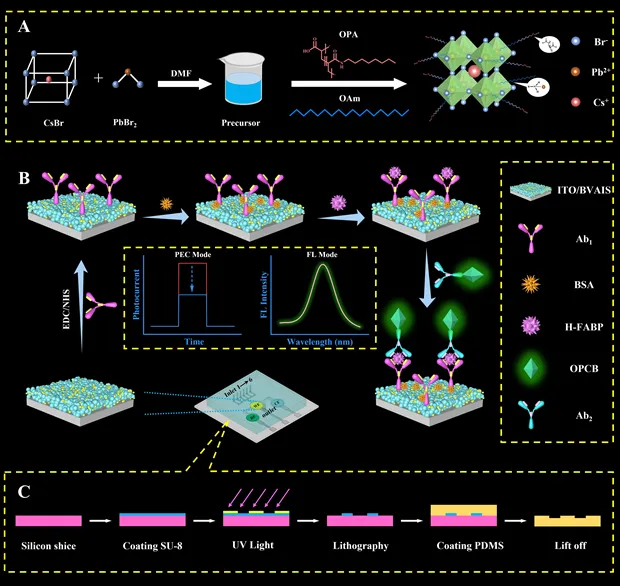
图1. (A)由两亲性配体OPA包覆的CsPbBr3纳米晶体的合成过程;(B)微流控传感平台的构建过程;(C)微流控通道制备流程。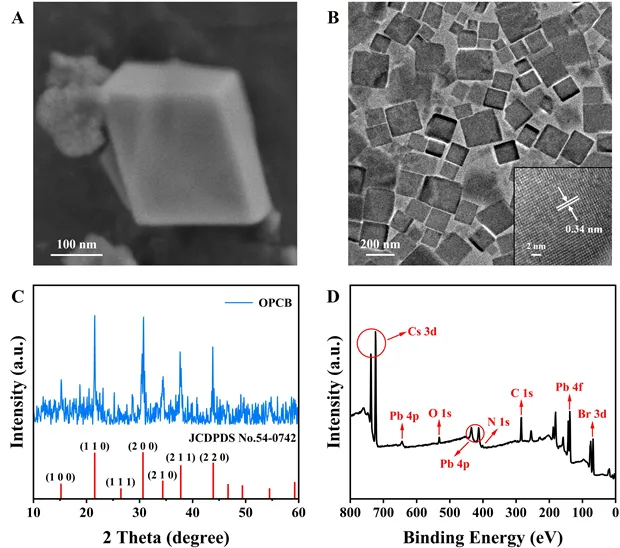
图2. OPA-CsPbBr3的(A)SEM图像、(B)TEM图像、(C)XRD谱图和(D)XPS谱图。通过紫外-可见光吸收光谱测试了纳米酶的抗坏血酸氧化酶活性,结果表明,OPCB能够成功氧化抗坏血酸。此外,利用邻苯二胺对纳米酶氧化抗坏血酸的产物进行验证,在420 nm处观察到明显的荧光发射峰,这是由于邻苯二胺与催化产物脱氢抗坏血酸结合生成具有荧光活性的DFQ。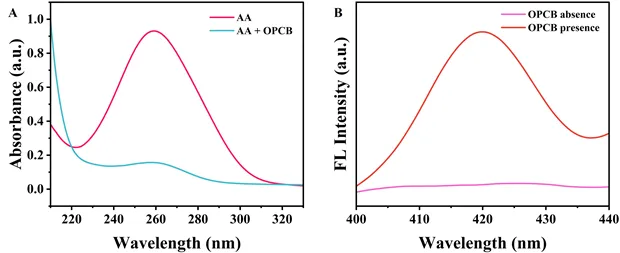
图3. (A) OPCB纳米酶存在和不存在时抗坏血酸的紫外-可见吸收光谱;(B) OPCB纳米酶存在和不存在时抗坏血酸+邻苯二胺溶液的荧光光谱。
随后,实现了对目标物H-FABP的PEC/FL检测,并对传感器的性能进行评估。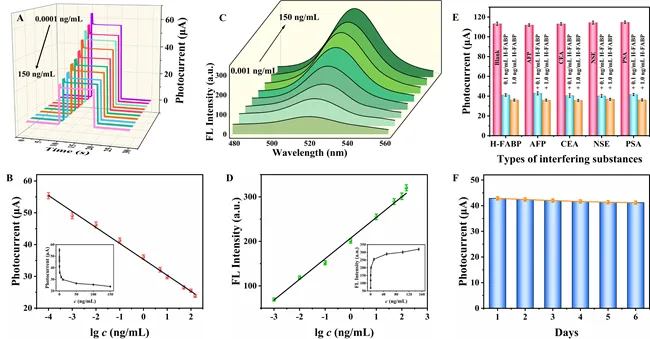
该研究为钙钛矿纳米酶在疾病诊断免疫传感器中的应用提供了新的视角,近期以" Advanced Dual-Mode Microfluidic Sensing Platform Based on
Amphiphilic Polymer-Capped Perovskite Nanozymes Induced Photoelectrochemical
Signal Amplification and Fluorescence Emission"为题发表在国际著名期刊Analytical
Chemistry上。论文第一作者为济南大学硕士研究生付军强。延伸阅读:
《即时诊断应用的生物传感器技术及市场-2022版》
《可穿戴传感器技术及市场-2025版》
《苹果在无创血糖监测领域的发明专利与产业布局分析》
《糖尿病管理技术及市场-2025版》