皮质脑电图(ECoG)是一种成熟的神经接口技术,通过电极阵列能够从皮层表面进行大面积神经记录。皮质脑电图通常用于癫痫发作定位,但是大面积皮质脑电图阵列的植入是一种高侵入性手术,需要进行大于植入面积的开颅手术才能部署该装置。
据麦姆斯咨询报道,近日,英国剑桥大学(University of Cambridge)、牛津大学(University of Oxford)和意大利博洛尼亚大学(University of Bologna)的研究人员组成的团队将柔性薄膜电极阵列与软体机器人概念相结合,实现了一种可通过集成流体驱动器改变形状的大面积皮质脑电图装置。研究表明,具有32个电极的装置可使用受折纸启发的折叠技术封装成压缩状态,并通过小钻孔开颅手术植入,然后在大脑表面展开以覆盖大面积的皮质。该装置的植入、展开和记录功能已在体外和猪体内模型中得到验证。将形状驱动集成到神经植入物中,为通过微创手术技术实现大面积神经接口提供了一条临床可行的途径。上述研究成果以“Origami-inspired soft fluidic actuation for minimally invasive large-area electrocorticography”为题发表于Nature Communications期刊。
微创皮质脑电图(MI-ECoG)装置的设计与制造
MI-ECoG装置是一种可折叠成小尺寸的大型、柔软的神经接口,可以通过钻孔开颅术将其插入到皮质表面的硬膜下。通过在MI-ECoG装置中心集成一个流体驱动腔室,可对该装置进行充气以驱动其原位展开,从而覆盖较大的皮质区域并实现神经记录(图1A)。薄膜制造技术被用于开发MI-ECoG装置,包括软光刻和光刻技术,以形成由硅树脂、聚对二甲苯-C、金和聚(3,4-乙烯二氧噻吩)聚苯乙烯磺酸盐(PEDOT:PSS)制成的装置(图1B)。MI-ECoG装置的完整横截面结构如图1C、1D所示。
为了在不进行全开颅手术的情况下将ECoG装置部署在硬膜下空间,该装置必须能够在狭窄的硬膜下空间内展开。图1E为用于封装和插入MI-ECoG的定制植入工具的图示。
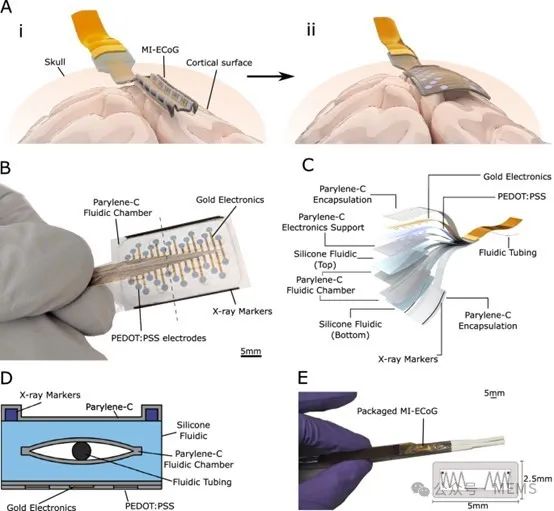
图1 受折纸启发的MI-ECoG装置的概述和设计
MI-ECoG装置的体外力学性能验证
鉴于MI-ECoG装置面临在有限的硬膜下空间内展开的挑战,需要对其进行体外力学性能验证。首先,研究人员研究了该装置所能承受的最大压力(图2A)。接着,他们使用水凝胶脑/硬脑膜模型对MI-ECoG装置的展开进行了体外测试,以确定合适的封装方法和可靠展开所需的流体压力。利用受折纸启发的手风琴形折叠封装该装置,流体驱动器可以驱动其在体外模型中完全展开(图2C、2D)。
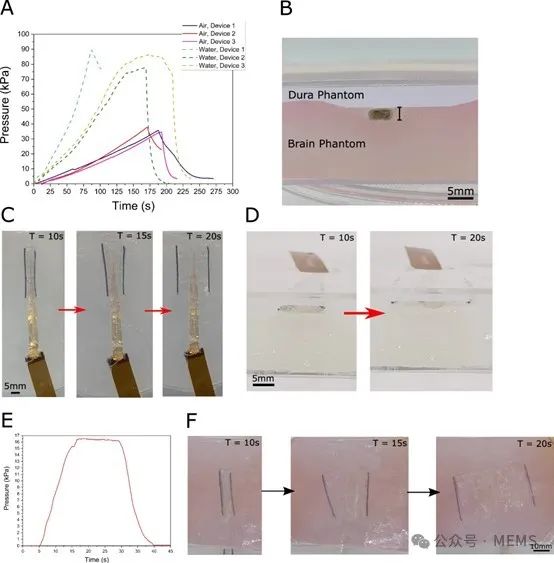
图2 水凝胶脑模中MI-ECoG装置的体外表征
MI-ECoG装置的猪体内验证
最后,研究人员使用50公斤左右的商业饲养猪来测试MI-ECoG装置在大脑皮层表面的植入和展开情况。开颅手术后,在硬脑膜上开一个6毫米的小切口,然后使用上述定制的插入工具将完全封装好的MI-ECoG插入皮质表面(图3A)。将折叠的MI-ECoG插入皮质表面并取出插入工具后,注射器被连接并耦合到压力传感器上。该装置被手动充气以驱动其在硬膜下空间的展开,如图3B所示。

图3 急性猪模型中MI-ECoG装置的体内植入和展开
成功植入后,完全展开的MI-ECoG被用于记录皮层脑活动。MI-ECoG被连接到Intan RHS刺激/记录系统,参考金电极放置在颅骨的皮下。同时,通过传统开颅手术在麻醉的猪皮层上植入一个16通道临床级PtIr ECoG,以便与MI-ECoG进行临床对比。测试结果表明,两者记录的皮层的听觉诱发电位(AEP)差异很小,并且功率密度谱和信噪比(SNR)相似(图3F、3G和3H)。研究人员还评估了MI-ECoG对脑表面的影响,目视检查和成像检查显示,MI-ECoG展开部位下方没有发现明显的形态变化或损伤。
综上所述,这项研究将软体机器人技术与生物电子学相结合,展示了一种微创硬膜下大面积皮质脑电波植入物(MI-ECoG)。通过改进流体驱动器设计,研究人员能够利用小钻孔开颅手术将受折纸启发的折叠ECoG引入硬膜下,然后通过形状驱动实现大面积皮质覆盖。完成部署后,MI-ECoG将完全展开并覆盖600平方毫米的皮质区域。MI-ECoG获得的AEP记录与使用传统植入的200微米厚硅PtIr箔ECoG获得的记录相当,其功率密度谱和信噪比也相似。这表明MI-ECoG在展开后与皮质表面有良好的接触,能够实现与传统植入阵列相似的电生理性能。
总之,这种微创设计范式有望使ECoG在临床上得到更广泛的应用,并开辟生物电子医学的新途径和此前由于手术风险未被探索的ECoG新应用。
论文链接:
https://doi.org/10.1038/s41467-024-50597-2


