
导读
红外高光谱成像通过结合成像和光谱学,可用于化学成分分布的表征和识别,在病毒检测和生物学分析中展现出强大优势。然而,由于低效率的光物质相互作用,传统红外高光谱成像在痕量检测和多物质识别方面存在技术瓶颈。表面声子极化激元具备强电磁场限制、长寿命和低损耗等优异光学性能,有望突破上述技术瓶颈,但其是否有助于高光谱成像以及如何赋能高光谱成像仍悬而未解。关键科学问题包括声子激发需克服动量不匹配,声子谐振受限于狭窄频率范围,以及声子系统存在强非线性等,这些因素提高了基于声子的高光谱成像的挑战性。
鉴于此,新加坡国立大学Chengkuo Lee(李正国)课题组开发了一种表面等离子体-声子超光谱成像系统,利用表面等离激元作为“桥梁”,克服了光子和声子模式之间的动量不匹配,拓宽了被限制在Reststrahlen带内声子谐振的带宽,构建了强非线性声子信号与分子折射率强度和线形特征的映射模型,实现了临床实验中的多种严重急性呼吸系统综合症冠状病毒(SARS-CoV)的超光谱成像。
该研究揭示了表面声子对超光谱成像的增强机制,证实了表面声子赋能超光谱成像以更强识别准确度、更高的灵敏度和更低的检测下限(低至病毒分子单层)。
相关研究成果以“Surface plasmons-phonons for mid-infrared hyperspectral imaging”为题,于2024年5月29日在线发表于国际顶级期刊Science Advances(Sci. Adv. 10 (22), eado3179, 2024)。同日,Science Advances以“特写图像”(Featured Image)形式和“Surface phonons enhance hyperspectral imaging”为题,对该研究在Science Advances网站首页进行了专题推介。新加坡国立大学博士后周鸿为论文第一作者,Chengkuo Lee教授为论文通讯作者。澳大利亚科学院院士、世界卫生组织COVID-19委员会委员、新加坡流行病防范和应对研究项目(PREPARE)首任执行主任Lin-Fa Wang教授参与了课题的联合攻关,并提供临床实验支持。

Science Advances网站首页专题推介
图源:Science Advances
红外高光谱成像在病毒检测和生物学分析中展现出强大优势。例如,严重急性呼吸综合症冠状病毒(SARS-CoV)是一种由核酸和蛋白质组成的冠状病毒。该病毒通过与宿主蛋白质相互作用,感染宿主细胞、复制病毒基因组并装配新病毒颗粒。研究新冠病毒蛋白质与宿主蛋白质的相互作用对于理解病毒生物学特性和寻找抗病毒药物靶点至关重要。红外高光谱成像凭借其谱学识别和成像能力,具备解析蛋白质相互作用的天然优势。
目前的红外高光谱成像在痕量(超低浓度)检测和多物质识别方面存在技术瓶颈。首先,弱的光-物质相互作用导致低浓度物质检测失效问题。根据朗伯比尔定律A(ω) = ∑Ni[ai(ω)cil],其中在特定频率ω处的总测量的吸收信号A取决于N种分子吸收率,浓度ci和光程长度l。由于低浓度样品具有非常小的l和ai (分子的红外吸收截面低, 一般仅为 10⁻²⁰ cm²),红外高光谱难以产生可辨别的样品成像信号。其次,物质之间的光谱重叠导致多物质识别失效问题。根据上述定律,多物质的吸收A可归因于三个参数中的任何一个或多个(ai, ci,和l)。因此,对于存在吸收光谱重叠的混合物,混合光谱无法提供各个分子的定量信息,即ai和ci解耦失效。
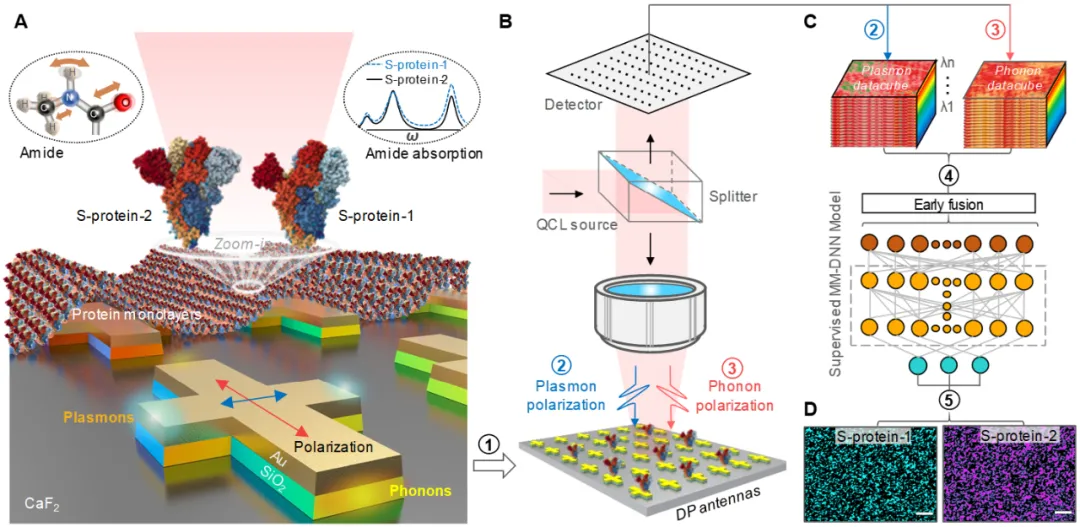
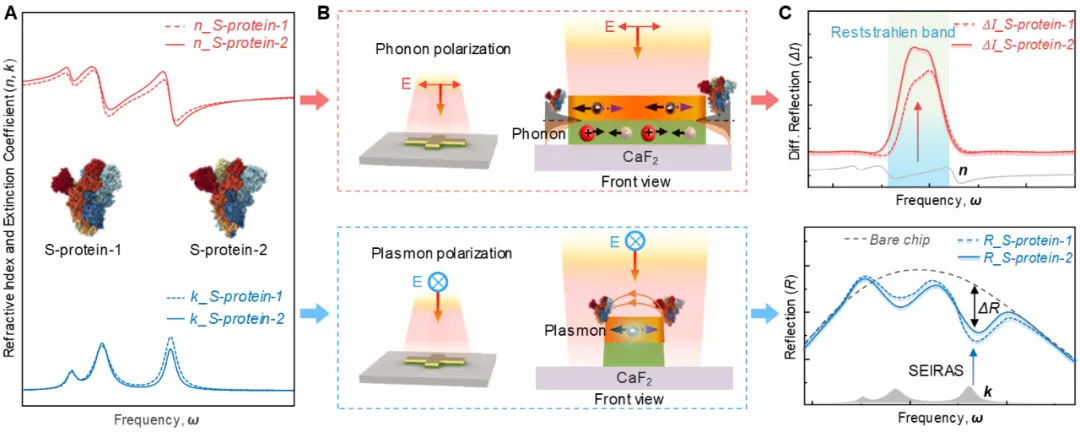
声子芯片与超光谱成像系统
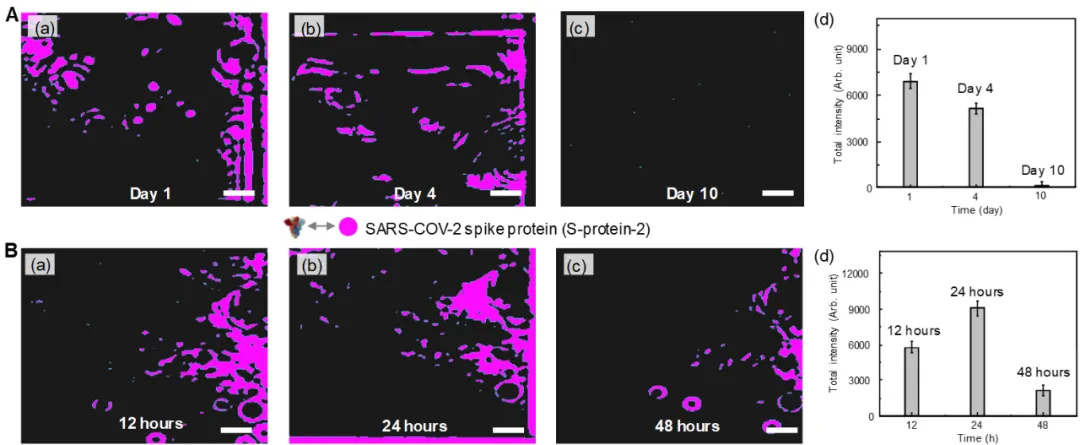
临床唾液样品中病毒单层的超光谱成像

总结与展望
论文信息:https://doi.org/10.1126/sciadv.ado3179


