点击左上角“锂电联盟会长”,即可关注!

本文作者:深北莫固态电池团队
全固态锂金属电池(ASSLMBs)具有较高的理论能量密度和安全性,被认为是最有希望的下一代电池技术之一。在众多的固态电解质(SE)材料中,富锂反钙钛矿(LiRAP)羟基卤氧化物具有易合成、低成本和易于扩大生产等优势,具有潜在的实际应用前景。尽管如此,仍然需要努力提升LiRAP的电化学性能来推进其实际应用。先前有研究人员发现,在含有聚阴离子的SE中,锂离子的传输与聚阴离子的旋转和重新定向运动密切相关,这增强了锂离子电导率并降低了活化能。然而目前含有聚阴离子的LiRAP在文献中还少见报道,聚阴离子对LiRAP的电化学性能和锂离子传输的影响仍然有待探索。
近日,深圳北理莫斯科大学卞均操副研究员、汕头大学邓贝副教授、宁波东方理工大学(暂名)赵予生教授和南方科技大学卢周广教授合作报道了一种三元聚阴离子的旋转耦合机制,可有效地促进锂离子的传输。实验发现在Li2OHCl中适当掺杂BF4-可以有效地提升锂离子电导率,降低活化能,降低电子电导率,增强对锂金属的电化学稳定性。第一性原理计算表明锂离子输运与OH–、BF4-和Li2–O–H八面体的强耦合旋转密切相关,这使锂离子电导率提高了1.8倍,活化能降低了0.03 eV。
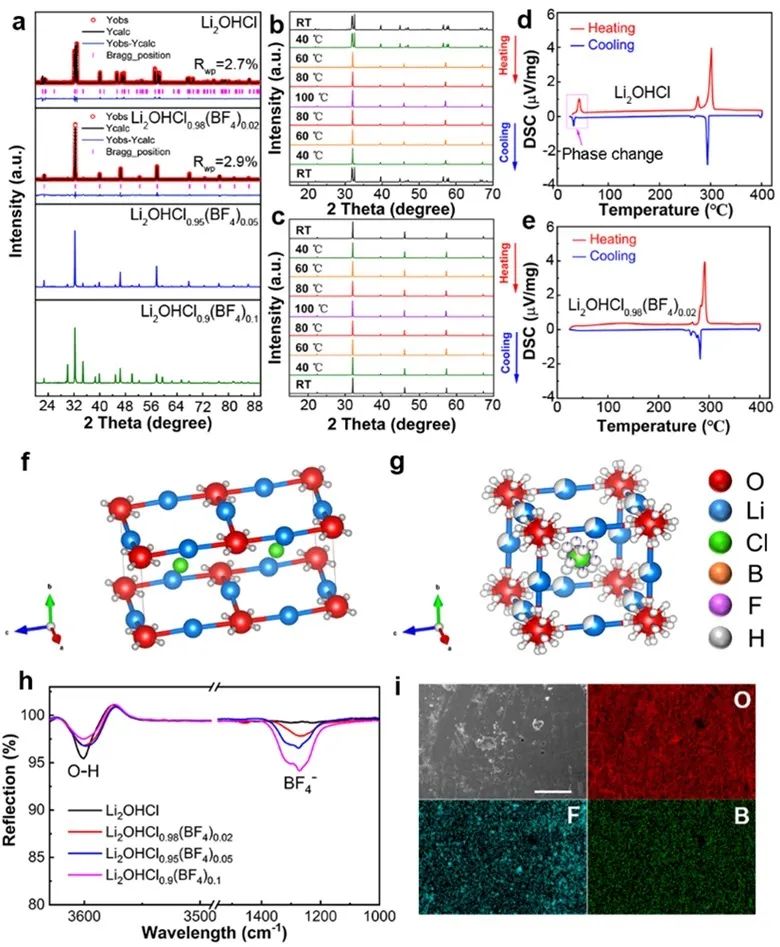
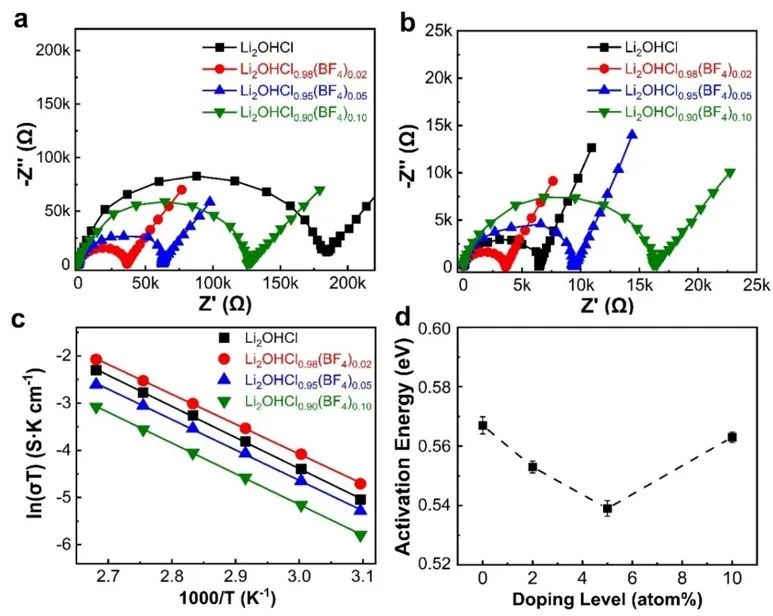
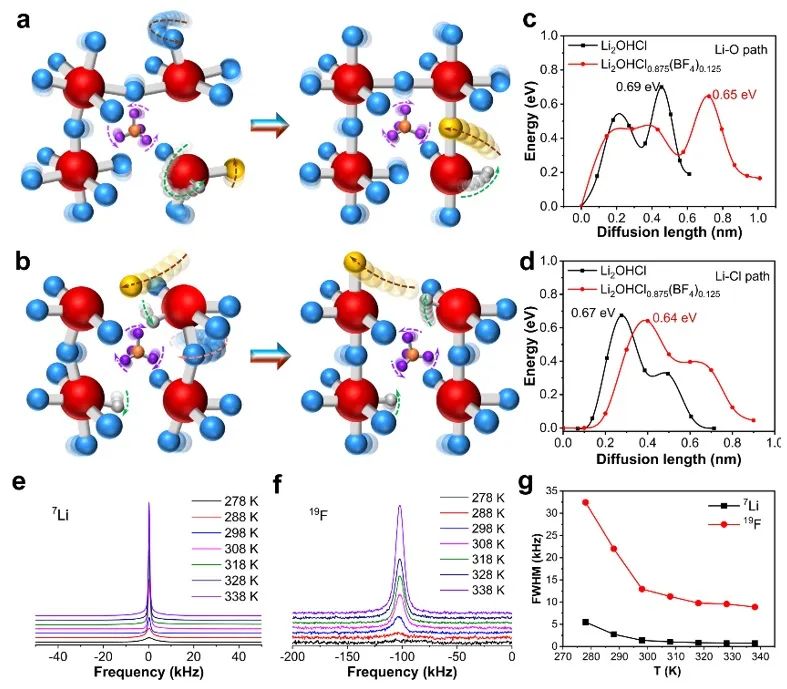
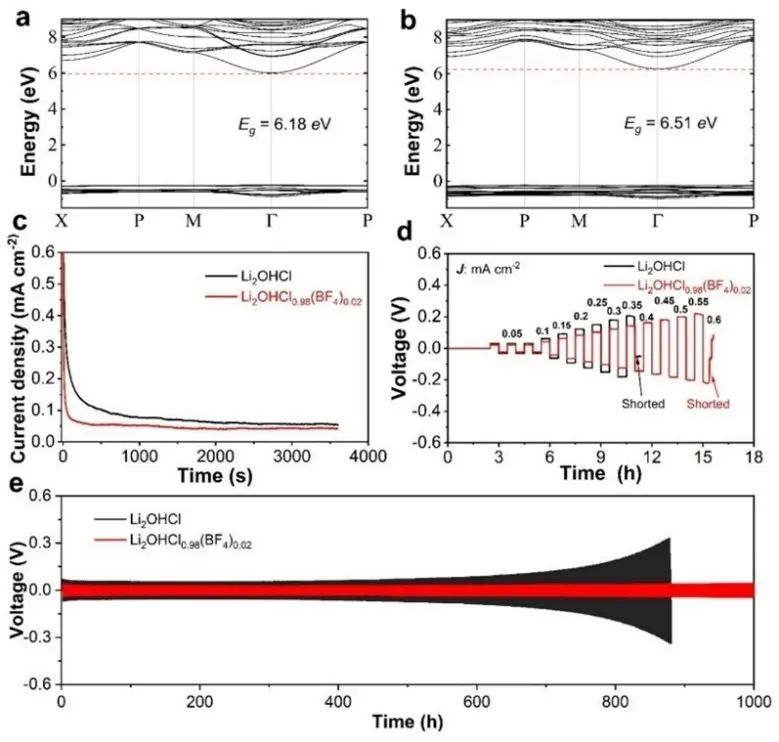
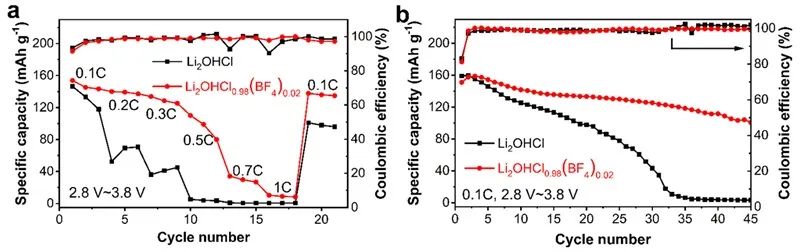
图1.(a)室温下Li2OHCl1-x(BF4)x(x=0、0.02、0.05和0.1)的PXRD。(b)Li2OHCl和(c)Li2OHCl0.98(BF4)0.02不同温度下的PXRD。(d)Li2OHCl和(e)Li2OHCl0.98(BF4)0.02的DSC曲线。(f)Li2OHCl和(g)Li2OHCl0.98(BF4)0.02的晶体结构。(h)Li2OHCl1-x(BF4)x的FTIR光谱。(i)EDS元素分布图,比例尺为50 μm。PXRD的结果显示Li2OHCl在室温下为正交相。变温PXRD显示,在40 ℃左右Li2OHCl发生了立方相和正交相之间的可逆相变。掺杂BF4-后,Li2OHCl1-x(BF4)x在不同温度下均表现为立方相。DSC曲线中也观察到了这种相变(如图1b和1c)。对于Li2OHCl,在40.6 ℃处存在吸热峰,在26 ℃处存在放热峰,对应于正交相和立方相之间的相变。室温PXRD精修得到的Li2OHCl和Li2OHCl0.98(BF4)0.02的晶体结构如图1f和图1g所示,Li2OHCl0.98(BF4)0.02中B占据Cl位,F环绕在B周围,占据Wyckoff 12j位。FTIR光谱(图1h)观察到了B-F键振动峰,其强度随着掺杂浓度的增加而增强。由于F具有强电负性,随着BF4-掺杂浓度的增加,O-H振动峰的强度逐渐减弱。EDS元素分布(图1i)显示O、F和B元素均匀分布,进一步说明成功掺杂了BF4-。图2.(a)室温和(b)50℃下,Li2OHCl1-x(BF4)x(x=0、0.02、0.05和0.1)的电化学阻抗谱。(c)阿伦尼乌兹曲线和(d)Li2OHCl1-x(BF4)x(x=0、0.02、0.05和0.1)的活化能。室温下Li2OHCl1-x(BF4)x(x=0.02、0.05和0.1)的离子电导率均高于Li2OHCl,其中Li2OHCl0.98(BF4)0.02的离子电导率是Li2OHCl的5.2倍。为了排除相变带来的影响,在50℃均为立方相的情况下,Li2OHCl0.98(BF4)0.02的离子电导率仍是Li2OHCl的1.8倍。不同BF4-含量LiRAP的活化能如图2d所示,Li2OHCl0.98(BF4)0.02较Li2OHCl下降0.03eV。以上结果证明BF4-离子的存在有利于锂离子的传导。图3. CI-NEB模拟Li2OHCl0.875(BF4)0.125中锂离子沿(a)Li-O和(b)Li-Cl路径的传输轨迹示意图。红色、蓝色、金色、灰色、紫色和橙色球体分别表示O、未追踪的Li、追踪的Li,H、F和B。(c)Li-O和(d)Li-Cl路径上,Li2OHCl0.875(BF4)0.125和Li2OHCl能量图景。(e)7Li和(f)19F与温度相关的静态NMR谱。(g)7Li和19F不同温度下的半峰宽。如图3a所示,CI-NEB模拟了锂离子沿Li-O面的传输轨迹。在Li2OHCl0.875(BF4)0.125中,锂离子的传输路径(图3a棕色箭头)具有0.65eV的较低能垒(图3c)。锂离子从初始晶格位置向相邻的晶格位置移动,并在初始位置留下了一个空位。同时,相邻的H围绕O原子旋转了约270°(绿色箭头),并最终占据了该空位。此外,近邻的BF4-也同时旋转了一定角度,最终又反向旋转回来(紫色箭头),这与相邻的Li2-O-H八面体的旋转(红色箭头)相关联,表现为“响应动力学”。F具有较大的电负性,它的旋转将对相邻的Li和H产生较强的库伦吸引。因此,这样的“三体响应动力学”在很大程度上降低Li和H之间的库仑排斥。两者之间库伦排斥的减弱使H拥有更大的旋转自由度,这抑制了H的“空间位阻效应”,从而降低了锂离子的迁移能垒。以上表明OH、BF4-和Li2-O-H八面体的旋转与锂离子的迁移具有强烈的耦合效应。锂离子沿Li-Cl面的传输轨迹如图3b所示,锂离子传输的轨迹为抛物线(图3b棕色箭头)。锂离子运动的同时,近邻的H和BF4-会发生旋转(绿色箭头表示H,紫色箭头表示BF4-),这调节了局域电场,有利于锂离子的传输。此外,BF4-的旋转还与Li2-O-H八面体的旋转相耦合(红色箭头),这进一步增强了锂离子的传输。以上再次证明了O-H、BF4-和Li2-O-H八面体的旋转是强烈耦合的,“三体响应动力学”同样协助了锂离子在Li-Cl面上的传输。静态NMR显示,在278k到318k的温度范围下,7Li和19F的FWHM迅速减小,这表明7Li-7Li和19F-19F相互作用减少,Li和F的运动更加活跃。温度升高一方面会提高离子的运动频率,另一方面也增加了聚阴离子的旋转自由度,这促进了O-H、BF4-和Li2-O-H八面体的旋转耦合。在较高温度时7Li的FWHM较窄,19F的FWHM仍保持较宽(~9.6 kHz),这表明F只能局域在B周围运动,而Li可以在晶体内长程传输。图4.(a)Li2OHCl和(b)Li2OHCl0.875(BF4)0.125的能带结构。(c)电子电导率测试(d)极限电流密度。(e)Li2OHCl和Li2OHCl0.98(BF4)0.02的Li//Li对称电池循环。Li2OHCl的带隙为6.18 eV,Li2OHCl0.875(BF4)0.125的带隙6.51 eV,这意味着Li2OHCl0.875(BF4)0.125的电子电导率将小于Li2OHCl,直流极化测试证明了这一点。电子电导率对固态电解质的极限电流密度起着关键作用,如图4e,Li2OHCl0.98(BF4)0.02的临界电流密度为0.60 mA cm-2,大于Li2OHCl(0.35 mA cm-2)。Li-Li对称电池的数据显示,Li2OHCl组装的对称电池在880 h短路,最终极化电压较循环前放大4.9倍。而Li2OHCl0.98(BF4)0.02组装的对称电池在1000 h仍保持稳定,1000 h时极化电压仅比初始时高14.5%。这是因为Li2OHCl0.98(BF4)0.02的LUMO能级上移,使Li2OHCl0.98(BF4)0.02具有更强的抗还原性,这增强了其与锂金属界面的稳定性。图5. Li2OHCl和Li2OHCl0.98(BF4)0.02全电池的倍率性能和循环表现LiFePO4//Li2OHCl0.98(BF4)0.02//Li全电池表现出了更好的倍率性能和循环性能。倍率性能的提升归因于掺杂BF4-后离子电导率的提升。使用Li2OHCl0.98(BF4)0.02装配的电池在0.1C下循环45次后具有66.7%的容量保持率,而使用Li2OHCl装配的电池在45次循环后仅剩下2.2%的容量,后者快速的容量衰减可归因于Li2OHCl较低的离子电导率和对锂金属较差的电化学稳定性。聚阴离子BF4-的掺杂影响了LiRAP SE中锂离子的动力学、相变、电化学稳定性和电子导电率,提高了ASSLMB的电化学性能。锂离子与BF4-、O-H和Li2-O-H八面体的动力学过程在空间和时间上是相关的。BF4-、O-H和Li2-O-H八面体运动的三元耦合有效地提高了锂离子电导率并降低了能垒,从而实现了“三体响应动力学”。BF4-的掺杂使LiRAP的带隙变宽并提高了LUMO能级,从而降低了电子电导率并增强了其抗还原能力,提高Li//Li对称电池的循环稳定性和临界电流密度,从而提高了ASSLMB的循环和倍率性能。本工作证明了聚阴离子可以成功地用于构建超离子导体,并为下一代SE的设计提供理论指导。Ternary Rotational Polyanion Coupling Enables Fast Li Ion Dynamics in Tetrafluoroborate Ion Doped Antiperovskite Li2OHCl Solid ElectrolyteJuncao Bian, Sifan Ling, Bei Deng, Haibin Lin, Ruo Zhao, Long Kong, Huimin Yuan, Jinlong Zhu, Songbai Han, Liping Wang, Ruiqin Zhang, Yusheng Zhao, Zhouguang LuAngew. Chem. Int. Ed., 2024, DOI: 10.1002/anie.202400144工艺,研发,机理和专利!软包电池方向重磅汇总资料分享!
搞懂锂电池阻抗谱(EIS)不容易,这篇综述值得一看!锂电池循环寿命研究汇总(附60份精品资料免费下载)