癌症疫苗以预防肿瘤生长、复发和转移为目标,因其具有唤醒宿主免疫力以对抗肿瘤细胞的“独特”能力而备受关注。与基于肿瘤特异性抗原(TSA)的疫苗的快速开发不同,基于细胞的疫苗由于提取困难、制备繁琐和耗时长,进展并不令人满意。然而,作为体内存在的天然成分,细胞具有固有的生物相容性,并具有许多难以人工复制的功能和信息。因此,基于细胞的疫苗是一种能够最大程度保留机体免疫相关性的治疗肿瘤的手段。到目前为止,基于细胞的肿瘤疫苗主要包括树突状细胞(DC)疫苗和肿瘤全细胞疫苗(TWV)。其中,具有全套肿瘤相关抗原(TAA)和TSA的TWV在引发抗肿瘤免疫反应以建立个性化癌症疫苗方面显示出巨大潜力。然而,辐照失活的肿瘤全细胞引起的免疫力不足以实现肿瘤抵抗。其他几种细胞工程制造TWV的方法,包括基因工程修饰、液氮冷冻方法、添加佐剂以及与光疗相结合,治疗效果仍有提高的空间。
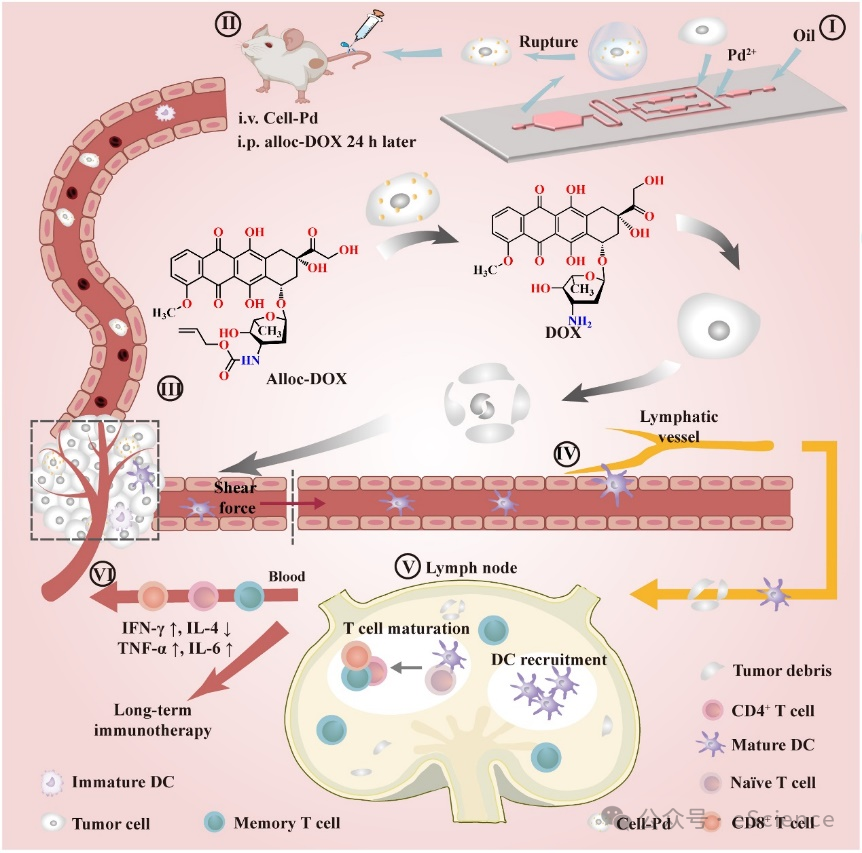
图1 微流控合成BCTWV用于催化抗肿瘤免疫治疗
液滴微流控芯片由三个模块组成:液滴生成、液滴观察和液滴收集模块。液滴产生模块包括三个入口、一个不对称蛇形系统和一个交叉流动结构,该结构产生大小均匀的液滴,其中含有癌症细胞和Pd²⁺。从芯片的出口收集产生的含有肿瘤细胞和Pd²⁺的液滴,在37℃下反应8小时后,破乳以收集金属化的细胞(图2)。
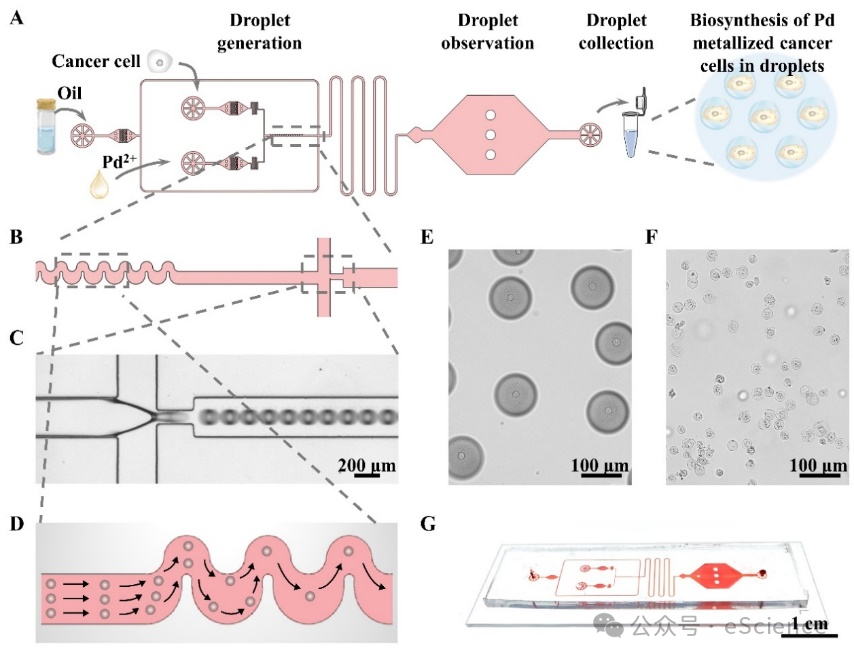
图2 微流控液滴中肿瘤细胞的矿化
扫描电子显微镜表明Cell-Pd保持完整的形状,透射电子显微镜观察到膜结构变暗,表明Pd纳米团簇(PdNCs)的生长。X射线光电子能谱显示,细胞中的PdNCs主要以Pd(0)的形式存在。Cell-Pd的催化性能利用RH110前药催化反应测试,催化系统的荧光显示出对Cell-Pd的浓度依赖性,并在观察时间内不断增加。为了研究Cell-Pd在体内的安全性,将Cell-Pd和活的4T1细胞静脉注射到小鼠中,并观察24天肿瘤的生长情况。与注射活4T1细胞的小鼠相比,Cell-Pd组的小鼠没有出现致癌的生物发光证据(图3)。
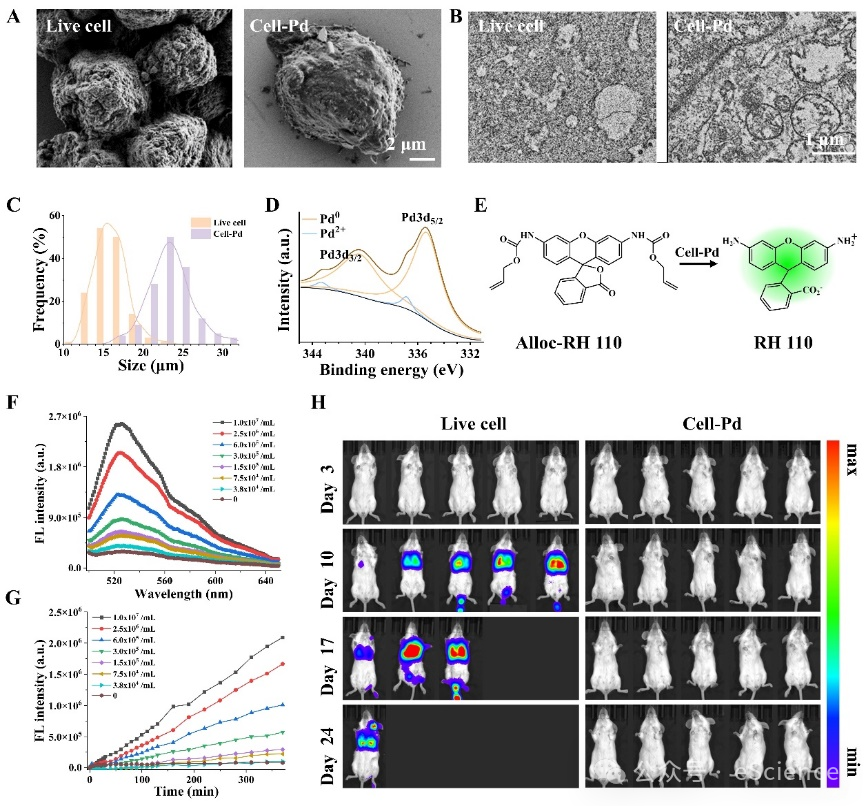
图3 Cell-Pd的表征
为了研究生物正交催化介导的免疫疗法的免疫机制,在荷瘤小鼠治疗的第15天取材量化DC的成熟度以及T细胞的表型进行免疫分析。Cell-Pd组和疫苗组中成熟DC比例增加,细胞毒性T细胞的肿瘤浸润增强,表明Cell-Pd可以诱导抗肿瘤免疫,并且Pd催化的生物正交反应可以显著增强机体的抗肿瘤免疫(图4)。
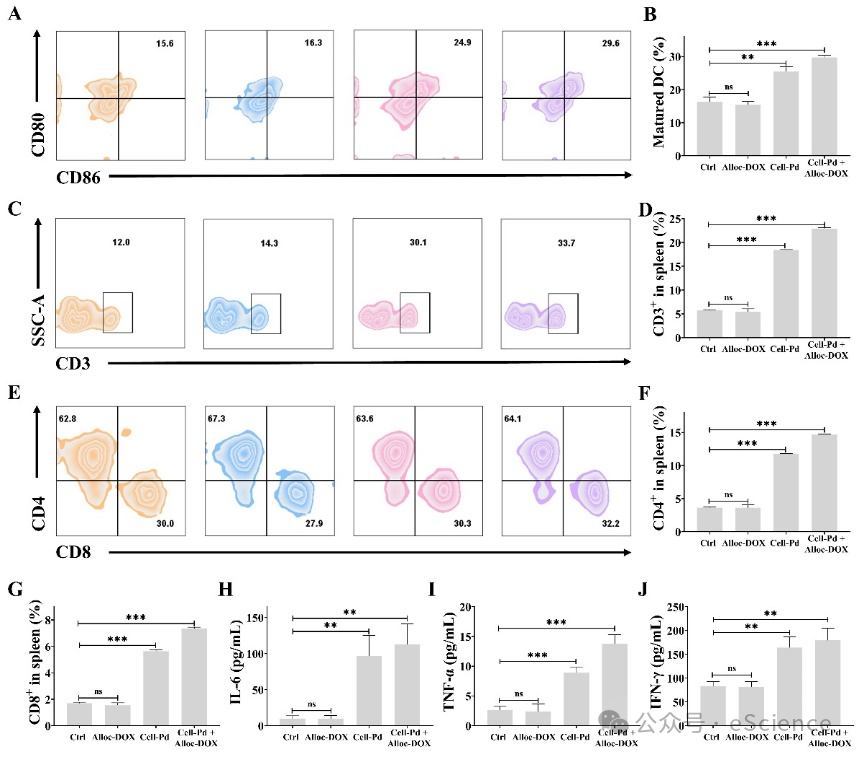
图4 BCTWV引起的抗肿瘤免疫


