流-固动态弯曲界面广泛存在于生物体内不同组织间或组织与管腔间,如血管、肠道、呼吸道和膀胱等,其在维持细胞功能和组织稳态等方面起着关键性作用。器官芯片能够通过构建包括活体细胞、组织成分、生物流体和组织形变等在内的各种器官微环境,体外再现生物体内的作用机制,在力学生物学、药物筛选等领域有广泛应用。然而,尚未有研究能够在器官芯片中再现组织流-固动态弯曲界面这一重要的生物力学环境,此外,如何在器官芯片中实现个性化力学微环境仍然存在挑战。
据麦姆斯咨询报道,近日,北京航空航天大学生物与医学工程学院、生物力学与力生物学教育部重点实验室、北京生物医学工程高精尖创新中心樊瑜波教授、刘肖副教授团队,以“Microfluidic Organ Chip of Fluid-Solid Dynamic Curved Interface”为题的文章发表于物理领域著名综合性期刊《Applied Physics Reviews》,并被选为期刊Featured article(特色文章)。美国物理学联合会《科学之光》(AIP Scilight)以“Flexible organ-on-a-chip device replicates complex curved surfaces”为题进行了报道。


该研究团队制造了一款具有三通道“分支”型流道结构设计的器官芯片,包含上层流道层、中间聚二甲基硅氧烷(PDMS)膜层和支撑基底层,并通过调控PDMS薄膜硬度成功模拟了不同组织的基底硬度。该芯片通过调控进入细胞培养通道和压力调节通道的流体流量,以及狭窄阻力通道的压力能够同时实现复杂的动态流动剪切力和循环应变力学环境的模拟(图1)。
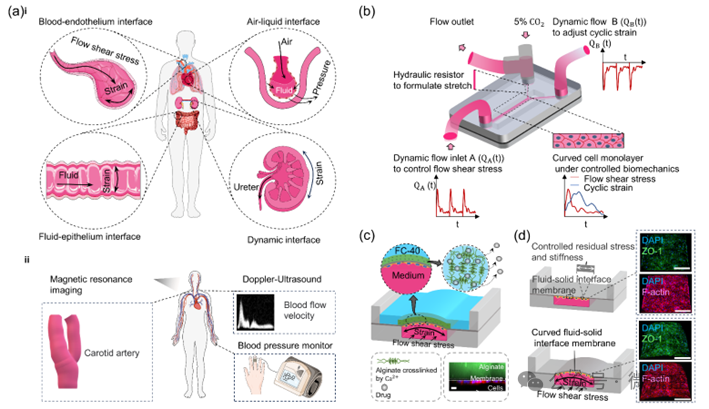
为精确控制器官芯片中的剪切应力和循环应变,研究团队应用纳维-斯托克斯方程和膜压力-变形关系方程,构建了剪切应力和应变与流量关系的理论分析模型,并利用三维建模仿真、粒子图像测速和光学相干断层扫描实验验证了理论模型的准确性。同时,该团队搭建了一套自动、高效、低能耗的流体灌注平台,可以实现灌注流量的精确控制(图2)。
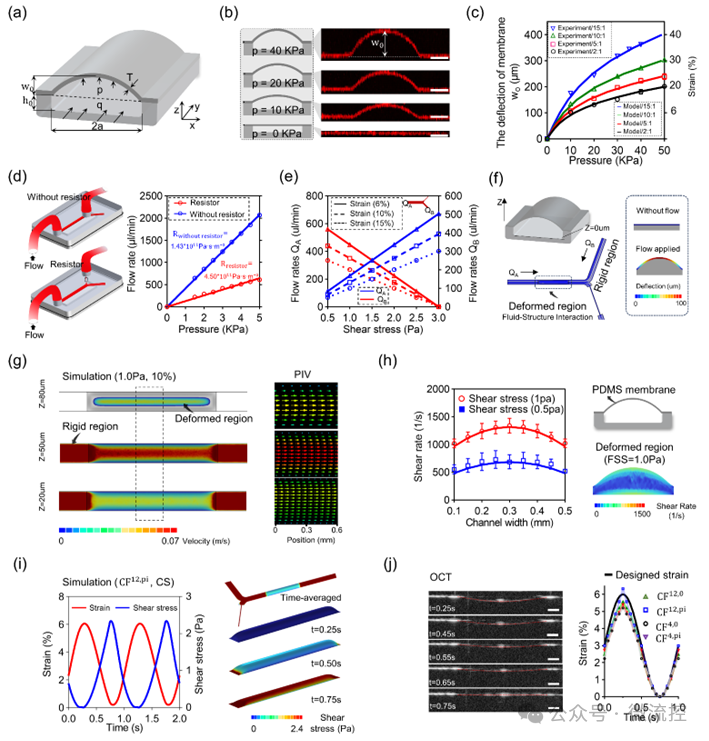
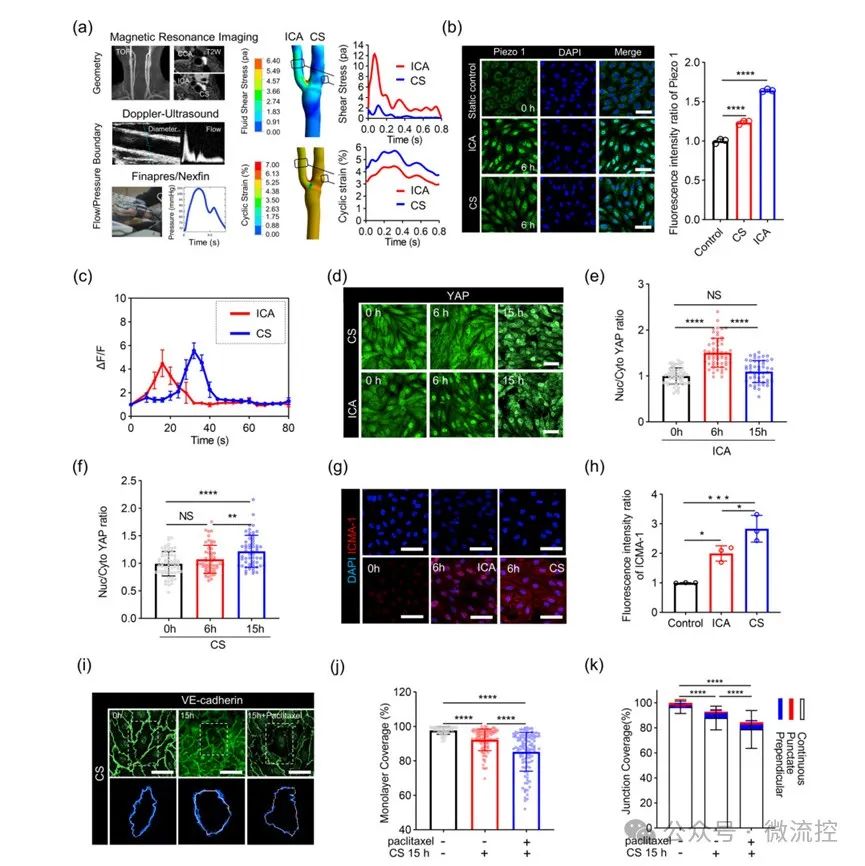
为验证该器官芯片的功效,该团队对多种力学环境条件下内皮细胞和上皮细胞的力传导机制进行了研究,测定了Ca²⁺跨膜转运通道Piezo1和力敏感转录因子YAP在芯片中的行为机制,展示了此器官芯片平台在模拟和研究细胞在生理或病理状态下行为机制的巨大潜力(图3)。
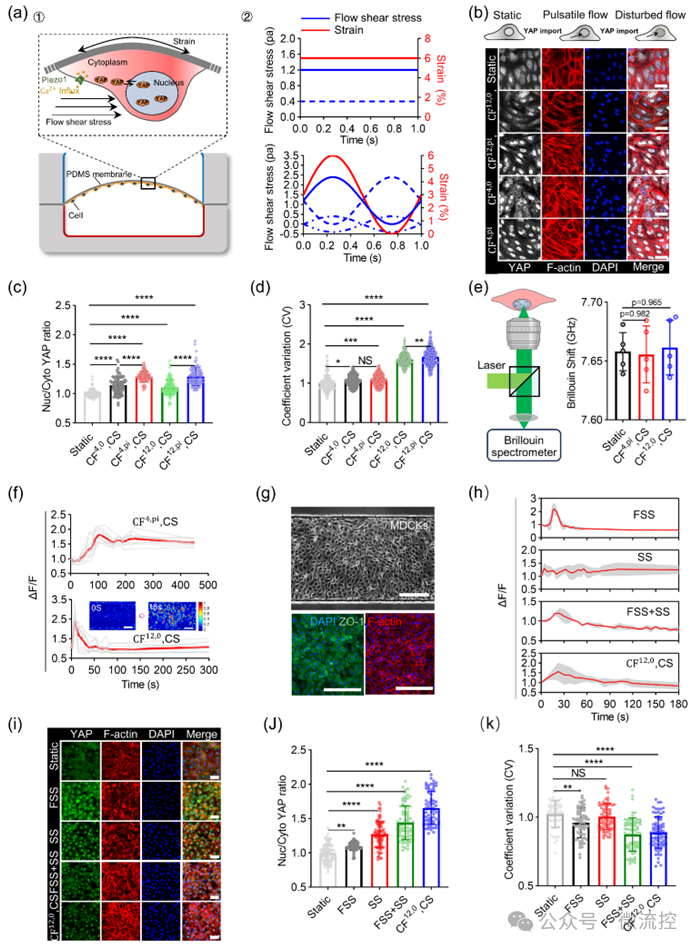
在此基础上,该团队还提出了一种创新的药物递送方式,使用藻酸盐包裹药物,在氯化钙溶液中实现交联,通过定量分析药物在藻酸盐中的释放过程和药物分子在PDMS薄膜中的扩散过程,实现了对药物剂量和释放速度的控制,为药物毒性测试和最佳剂量反应提供了新的途径(图4)。
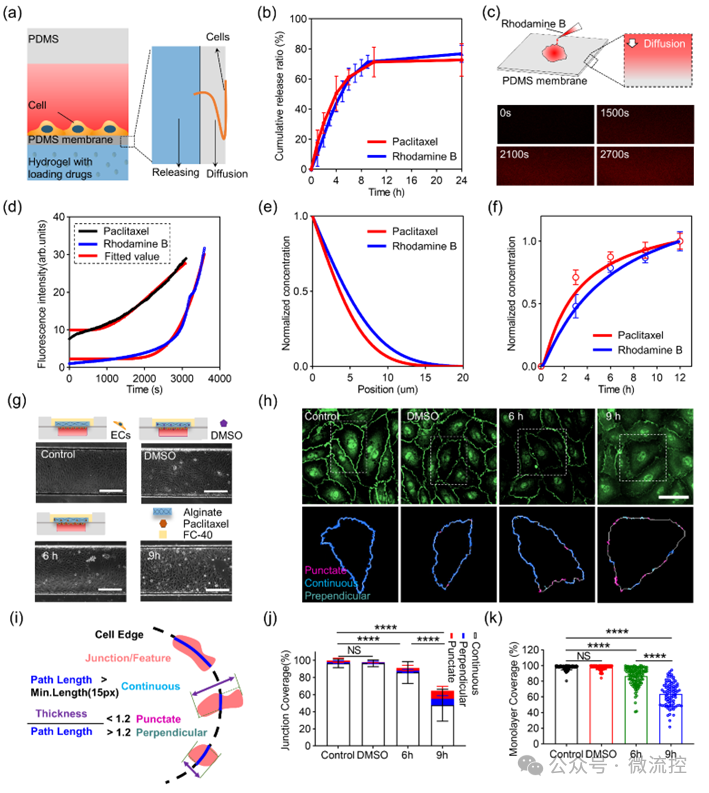
最后,该团队还对颈动脉个性化医疗方案进行探索(图5):通过影像学技术和多种检测手段获得颈动脉三维结构和力学边界条件,仿真计算出流动剪切力和循环应变分布;随后,根据前述理论分析模型,计算器官芯片模拟颈动脉窦和颈内动脉分支力环境所需要的灌注流量;进一步,结合流体灌注系统和药物释放系统,测试药物毒性和最佳剂量反应。这项工作为精准医疗的发展开辟了新的可能性,可通过此器官芯片平台,根据患者的个人生理、病理特征,量身定制药物治疗方案。
北航樊瑜波教授、刘肖副教授为该论文通讯作者,博士研究生苏皓然为该论文第一作者,北京航空航天大学为第一完成单位。本论文共同作者王立副教授、张靖教授、以及新墨西哥州立大学机械与航空航天工程系束方军教授,中国人民解放军第306医院王敏副主任,北京同仁医院眼科中心青光眼科辛晨副主任,国家干细胞工程技术研究中心张宇博士也对本论文做出了重要贡献。本项工作得到了北京市生物医学工程高精尖创新中心的平台条件支持,还得到了国家自然科学基金委(11827803, 31971244, 32371375, U20A20390和T2288101)、中央高校基础科研业务费(KG16186101)及“生物力学与力生物学创新引智基地”(111引智计划,B13003)等项目资助。


