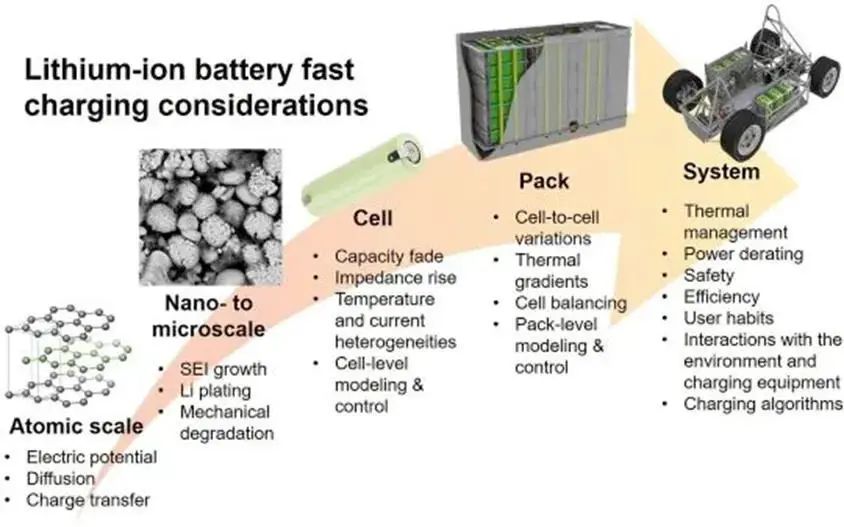
对于终端用户充电的基本诉求: 1)充电要快 2)不要影响电芯寿命 3)尽量省钱,充电机放出来多少电,尽量都充到我的电池里。
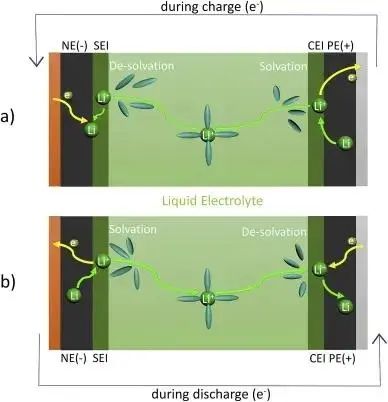
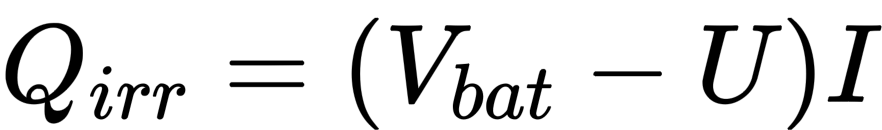
U为开路电压,Vbat为电池电压,I为电流(充电时)。
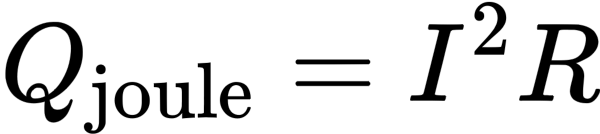
其中R为电池内阻。焦耳热与电流的平方成正比,因此快充时电流增大,不可逆热会显著增加。
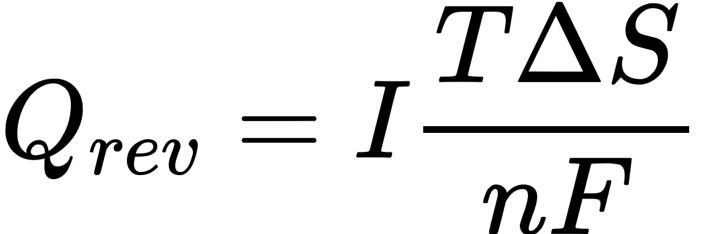
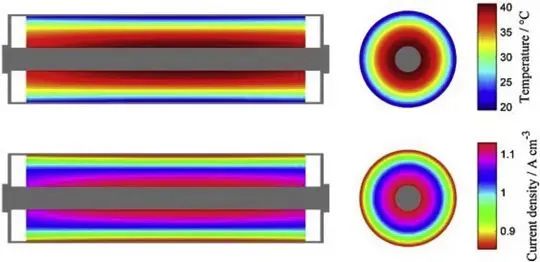
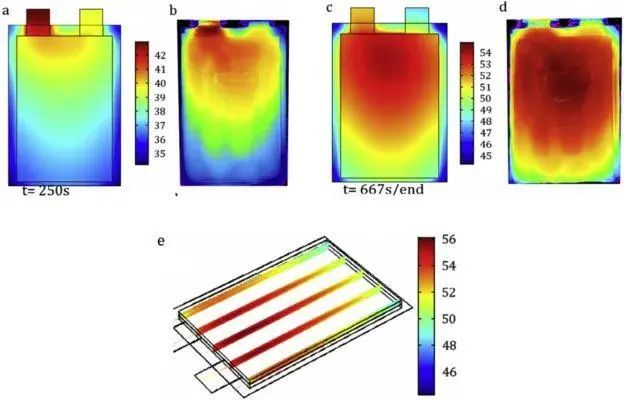
软包电池在5C恒流放电时的表面温度变化:t=250s的a)仿真结果和b)测量结果;t=667s的 c)仿真结果和 d)测量结果;e)内部温度的3D分布
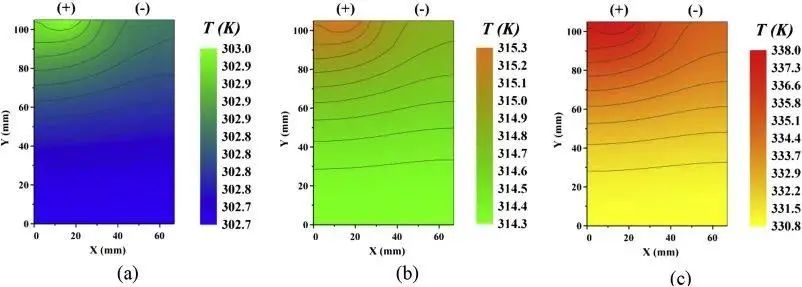
研究者们提出一些析锂观测的模型。包括Fuller,Doyle和Newman基于P2D模型的析锂模型,以及Arora,Doyle和White提出的可逆锂的嵌回过程。在此基础上,Perkins提出了面向控制的降阶模型;Hein和Latz提出了三维微观结构解析模型。Ren同时考虑了可逆锂的重嵌以及不可逆锂(死锂)在电池充电过程的反应。
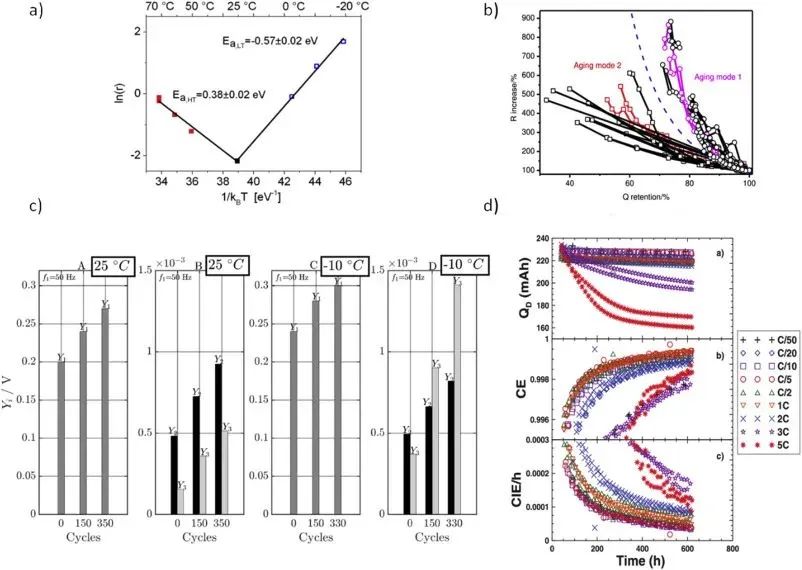
充电结束后的弛豫过程或紧接的放电过程会产生新的电压平台,如图7所示。电压微分(DVA)和容量微分(ICA)有助于寻找电压平台,但这些方法需要小倍率的放电,大电流会增大极化,覆盖电压曲线上的析锂信号。锂析出和重新嵌入的过程也可能会引起异常的产热峰值,作为析锂的信号之一。
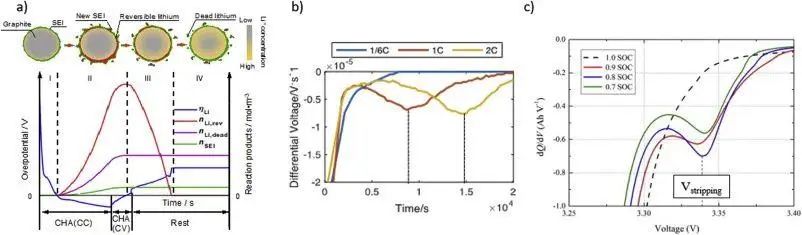
a)CC-CV充电和静置过程中的过电势变化模拟。 阶段I,负极颗粒上没有锂沉积; 阶段II,锂沉积开始发生; 阶段III,部分可逆的锂重新嵌入负极或溶出,剩余的变成死锂; 阶段IV,平衡态,死锂不再参与后续循环; b) 电压微分分析(DVA); c)微分容量分析(ICA)
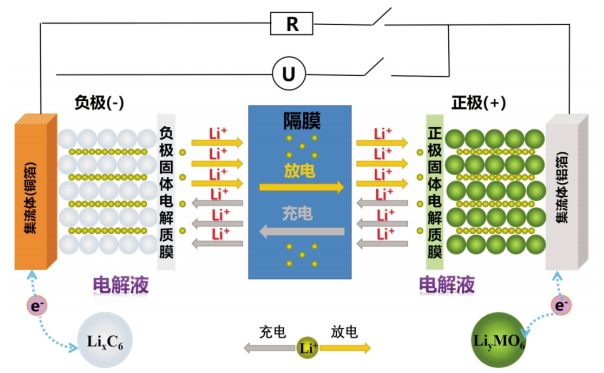
目前常用表面包覆改性来改善材料的性能。软硬碳的层间距比石墨稍大,有利于锂离子的扩散,通常石墨表层包覆软硬碳改善石墨的电化学性能,即通过表面修饰作用,在石墨表面形成无定形结构的碳层,增加了锂离子通道,改善锂离子扩散,提升其倍率性能。在设计快充型锂离子电池时,通常采用小颗粒以及软硬碳包覆的负极材料(提升负极脱嵌锂速度)。 改善负极材料的另一种方法是加快锂离子在负极材料中的扩散速度。比较有效的方法是制备具有多通道石墨负极材料,确保电解液能够充分浸润负极材料,并且缩短锂离子传输路程,达到提高锂离子扩散速度的目的。
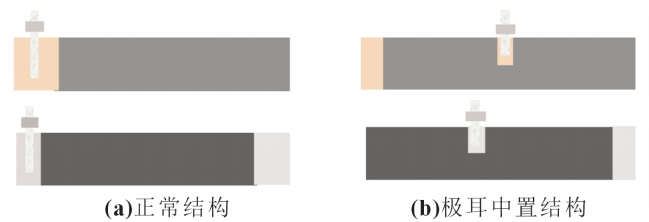
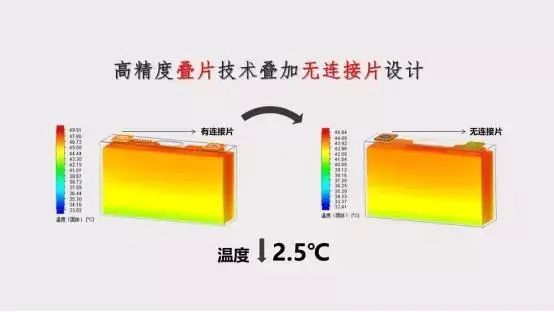
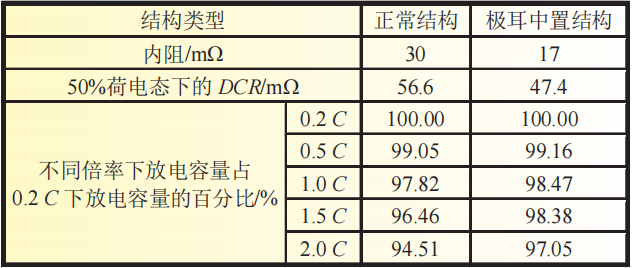
表1为两种结构的电池性能差异,同一型号采用极耳中置结构以及非极耳中置结构电池内阻、直流电阻(DCR)相差较大,常规结构内阻达到30mΩ,极耳中置结构内阻只有17mΩ;50%荷电态下常规结构的DCR为56.6mΩ,极耳中置结构为47.4mΩ。
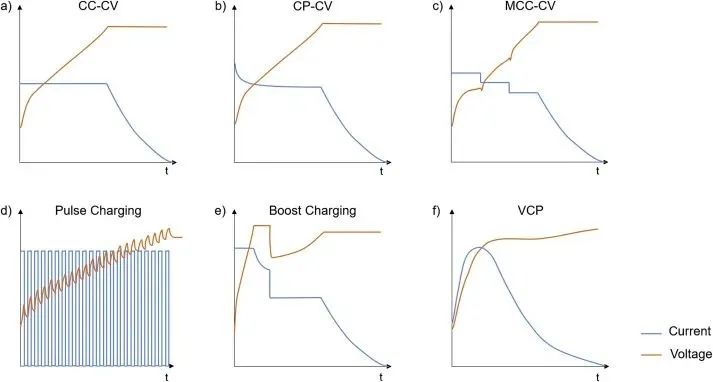
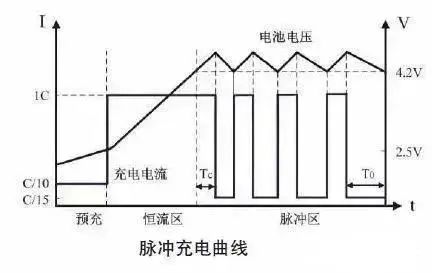
a)恒流-恒压(CC-CV); b)恒功率-恒压(CP-CV); c)多阶段恒流-恒压(MCC-CV); d)脉冲充电; e)CC-CV-CC-CV模式持续充电(Boostcharging); f)变电流充电(VCP)
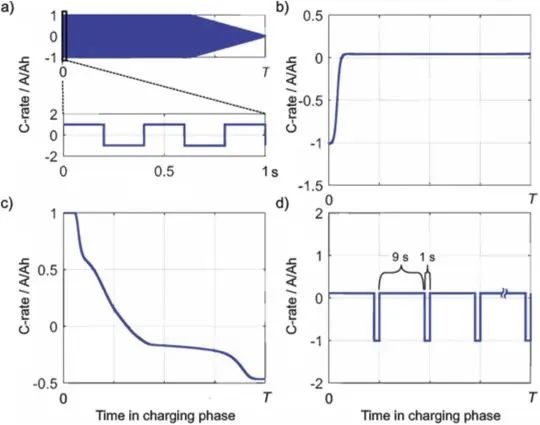
Schindler将图14不同充电策略结合对电池进行循环实验,并与CC-CV对比,研究电池在不同循环下的容量衰减。结果表明,结合所有充电策略进行循环实验,电池在800次循环后保持80%的容量,在所有循环中表现最好;只有CC-CV循环的电池衰减到相同容量仅用了400次;而CC-CV和冷降额结合的循环下,电池仅循环了330次,表现最差。
1)自放电加热。这种方法效率较低; 2)电池驱动电热丝并配合风扇加热。这种方法加热速度相对较快但效率还不够高且加热不均匀; 3)双向脉冲加热。即将一个电池Pack分为两组等容量的电池,电量在两组电池之间进行脉冲交换,利用内阻进行加热。这种方法效率较高,主要受DC/DC转换的限制,仿真结果表明此方法可以在120s内将2.2Ah的18650电池从-20℃加热到20℃; 4)交流电加热。这种加热的方法更快,但其对电池老化和循环稳定性的影响尚不明确。设计锂离子电池构型以实现快速预加热也是解决低温快充的途径之一。例如,可以在两层单面的负极层中间插入电化学分离的镍箔,通过开关控制直流电流流经镍箔进行快速加热。
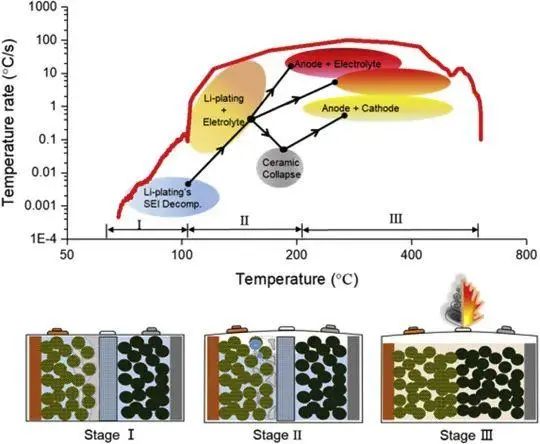
第一阶段(60℃ < T< 110℃),析出的锂与电解液反应加热电池,SEI膜不断破裂与再生,此时温度相对较低。 第二阶段(热失控诱发阶段),锂金属在与电解液的反应中被大量消耗,造成温度急剧升高。隔膜收缩,正负极接触。 第三阶段(热失控至最高温度),由于温度突然升高,正负极与电解液及正负极之间开始发生反应。最终电池温度达到最高并发生热失控。
阶段1(100% < SOC < 120%):电压超过充电截止电压后开始缓慢增加,此时过量的负极材料还能正常嵌锂以保证安全性。电池材料的一些副反应可能会被诱发,电池内阻和温度有轻微增加。 阶段2(120% < SOC < 140%):由于过度脱锂,正极的过渡金属离子例如Mn2+开始溶解。同时由于电压超出了电解液的电化学窗口,电解液也开始发生氧化。负极无法接收更多的锂离子开始不稳定并发生析锂,锂金属与电解液反应形成新的SEI膜,增加电池内阻。过充产生的焦耳热会使电池温度显著增加。 阶段3(140% < SOC < 160%):电池材料的放热反应迅速赶上并超过的电流的焦耳产热,并成为主要的产热方式。电解液氧化大量产热并伴随着产气,造成电池包膨胀。随着析锂量的增加,其与电解液的副反应也更加剧烈。SOC接近160%时,正极中的Mn2+大量溶解。正极结构开始变化,电池电压达到最大值并开始逐渐降低。 阶段4 (140% < SOC < 160%):电解液分解大量产气导致电池包突然破裂。隔膜破裂,电池内部发生大面积内短路,最终电池发生热失控。
1)将电解液的氧化电位从4.4V提升至4.7V,这可以使电解液更稳定,发生热失控的SOC增加至183%。向电解液中加入功能添加剂或能发生可逆氧化还原反应的添加剂可以实现这一目标。 2)将电池热失控温度提升至300℃以延缓大面积内短路的发生,发生热失控的SOC增加至180%。通过优化电池的压力设计,或使用高热交换稳定性的隔膜,可以延缓电池包的破裂。