疾病的诊断和监测常常通过检测血液、尿液、唾液和其它体液中的生物标志物来实现。特别是包围着体内细胞和组织的间质液(ISF),是一种丰富的生物标志物来源。由于间质液中不含任何颗粒,并且运输的蛋白质比血清中运输的蛋白质少,因此有利于生物传感应用。此外,与其它体液相比,间质液中同时含有系统性生物标志物和特异性生物标志物。然而,收集间质液的困难限制了其在临床和研究中的应用。获取间质液对于促进新的生物标志物的发现、更有效的医疗保健以及对不同疾病的早期诊断和监测非常重要。就速度和安全性方面而言,通过皮肤来收集间质液是最佳方式。由于皮肤是最容易接触的器官,因而是一个有效的间质液来源。通过皮肤提取间质液的方法有多种,如植入式毛细管法、微移液管插入法和水泡法等。目前,这些方法正逐渐被微针(MNs)的使用所取代。微针具有更强的以微创方式获取生物信息的能力,并且具有无痛、耐受性好、易于使用和有效的优势。
微针是一种具有微米级特征尺寸的装置,能够物理破坏角质层(SC),即皮肤的外层。微针的长度为数百微米,尖端锋利,通常以阵列形式组装在贴片上,并且,组装后的微针贴片可以轻松贴在皮肤上。不同类型的微针,如实心微针、溶胀微针和空心微针都可以用作传感器。其中,空心微针(HMNs)具有内置腔体,可以作为有效的生物流体收集器,在真皮层和皮肤外层之间的界面上创建透皮流体路径。此外,空心微针通常与吸液纸集成,集成后的装置能够收集间质液,以用于后续的化学分析。然而,通过空心微针装置收集的间质液通常需要在额外的独立装置中进行分析,从而需要引入额外的间质液转移步骤,即将纸基微针贴片在萃取介质中进行孵育,并通过离心从中提取分析物,而后再用适当的分析方法对提取出的分析物进行检测。总而言之,这些装置需要将收集到的间质液从微针管腔转移到分析物检测器。这通常使得微针装置只能以较长的时间提取少量可使用的间质液,从而进一步导致传感器响应的缓慢。
据麦姆斯咨询报道,为了克服以上微针技术的局限性,意大利国家研究委员会应用科学和智能系统研究所(ISASI)的研究人员提出了一种空心微针贴片装置,该装置的微针空腔中填充了含有金纳米颗粒(AuNPs)的高度溶胀聚乙二醇二丙烯酸酯(PEGDA)3D网络结构,从而构建了一种等离子体传感器。该微针装置可以直接检测提取的生物标志物,无需任何额外的步骤。该基于高分子量(Mw)PEGDA和球形金纳米颗粒的3D光学传感器集成了以下几个优点,例如,在空心微针腔内具有良好的适应性和灵活性,更高的表面积以及表面积体积比,并且不需要复杂的电路(因为与皮肤接触会产生干扰,复杂电路的需求通常是可穿戴生物传感器应用的瓶颈)。相关研究成果以“Hollow Microneedle-based Plasmonic Sensor for on Patch Detection of Molecules in Dermal Interstitial Fluid”为题发表于Advanced Materials期刊。
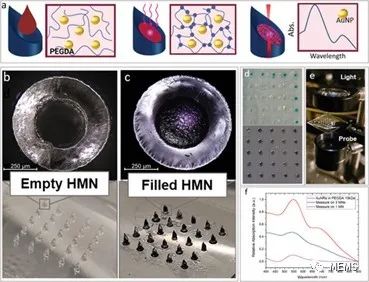
等离子体纳米复合材料在空心微针阵列腔内的集成
该空心微针贴片通过光刻方法制造,并利用了PEGDA在低分子量下的光交联特性。PEGDA是一种具有生物相容性的无毒聚合物。将金纳米颗粒包裹在高分子量PEGDA中,然后插入到空心微针腔中。随后,利用高分子量PEGDA的高溶胀特性提取间质液。该技术避免了对收集的间质液进行独立分析,并允许直接从微针装置检测感兴趣的靶分子。
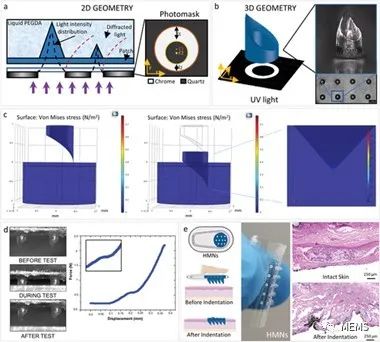
空心微针阵列的制备与表征
此外,该微针传感装置利用金纳米颗粒作为光学换能器,该换能器的原理是基于局部表面等离子体共振(LSPR)现象,该现象是由特定激发波长下纳米颗粒表面电子密度的振荡引起的。与此同时,如果满足合适的条件,金纳米颗粒周围的电磁场增强可以导致荧光团的强荧光增强。这种现象被称为金属增强荧光(MEF)或等离子体增强荧光,通常用于将等离子体生物传感器的检测极限(LOD)提高到单分子水平。因此,设计并制作的基于高分子量PEGDA和球形金纳米颗粒的等离子体纳米复合换能器可在双光学模式下工作。随后,为了进行概念验证,研究人员利用生物素-链霉亲和素的相互结合作用构建靶/受体耦联系统,在溶液中测试了集成等离子体空心微针装置的传感性能。
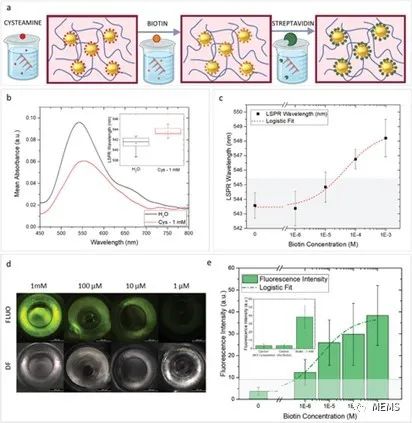
等离子体空心微针阵列对生物素-链霉亲和素相互结合作用的双光学模式传感
最后,研究人员通过使用由封口膜和琼脂(分别用于模拟角质层和真皮层)制成的皮肤模型,测试了所提出的装置从皮肤中收集和捕获生物素靶分子的能力。测试结果表明,无论是利用无标记的LSPR传感机制还是基于荧光的传感机制,作为靶标的生物素,都可以被成功地检索和光学检测,从而证明了本文所提出平台的功能有效性。

从皮肤模型中提取和检测生物素的概念验证工作
综上所述,该研究开发的等离子体空心微针可以作为开发一种简单、低成本、可大规模推广和通用的使用点(point-of-use,PoU)检测装置工作的起点,可以替代传统的、昂贵的、费力的医院或实验室装置,用于监测患者体内间质液中的生物标志物。此外,通过利用不同形状的纳米颗粒(例如纳米棱柱、纳米三角形和/或纳米星形)以及其尖端形状现象,或者通过增加换能器体积从而增加收集的间质液体积,可以进一步提升小分子的无标记检测性能。由于人口老龄化以及专业人员和医院床位的缺乏,这些PoU检测装置正受到越来越多的关注。因此,对PoU装置的需求变得越来越迫切,所提出的方法可以为满足这一需求铺平道路。
论文链接:
https://doi.org/10.1002/admt.202300037






