印刷生物传感器可实现对生物体细胞到器官各个水平的检测与传感,在医学研究领域具有广泛的应用前景。直接打印技术(DIW)可在各种生物基材上进行快速原型设计和定制具有几何复杂性的多功能生物传感器。这种方法消除了对传统基于光刻技术通常需要的多个步骤、掩模和专用工具的需求。DIW使用导电聚合物油墨或含有导电纳米填充剂的有机硅复合油墨作为打印原料,为此,需要精确控制油墨的流变学性质,以实现(1)高精度印刷适应性,以便在微尺度上进行复杂的渲染;(2)防止高密度分散的纳米填料发生聚合以阻碍油墨正常流动。然而,这些油墨由于其粘弹性性质,在周期性大应变下表现出机械和电气滞后,并且由于难以维持导电纳米填料的渗透网络而导致导电性不可逆的降解。此外,由于界面处的低相互作用能及其固有弹性的差异,粘弹性油墨在大变形下可能会产生生物相容性基材分层的现象。这些油墨的根本局限性阻碍了它们在医学上的实际应用,特别是在需要对重复负荷进行可靠记录的条件下,例如心脏跳动。
据麦姆斯咨询报道,基于以上问题,美国普渡大学西拉法叶分校机械工程学院(School of Mechanical Engineering,Purdue University,West Lafayette)的研究人员制备了一种海绵状形式的多孔柔性有机硅复合材料,具有优异的流变性能,可实现微量级DIW。进一步研究发现,该复合材料其具有优异的可逆可压缩弹性,可有效抑制重复加载循环中机械和电气的滞后。同时,其具有超低的模量(E<30kPa)和优异的柔性,与人类心脏组织(29-41kPa)相当。相关研究成果以“Rapid custom prototyping of soft poroelastic biosensor for simultaneous epicardial recording and imaging”为题发表在期刊Nature Communications上。
具体来看,研究人员首先通过非侵入性超声成像对心肌进行四维(4D)分割(即心脏周期上的3D几何体积),捕获心脏梗死区域的整体大小,几何形状和结构(图1a),然后,在120°C的加压热蒸汽条件下,将预聚物油墨的选择性图案化痕迹聚合成孔径为5-50μm的无定形海绵状形态,并在其中加入Ag片,最后,再加入油墨,填充网格,并用PVA薄膜将器件从Si片上剥离下来,然后使用剪刀修剪以去除多余的区域(图1b-e)。
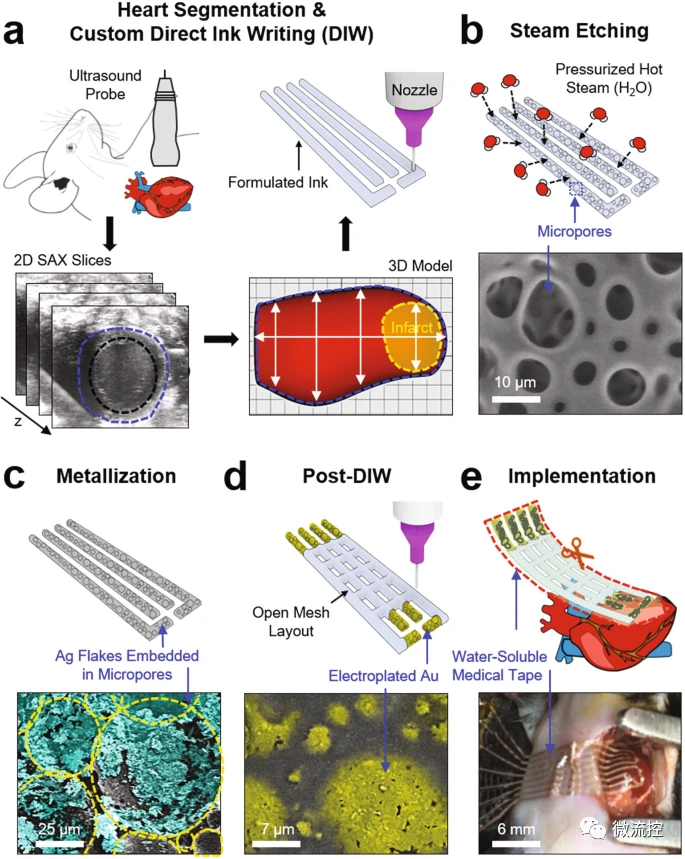
图1 多孔柔性生物传感器关键工艺步骤和光学图像
DIW使用的油墨的流变特性是控制印刷设备印刷适应性和结构完整性的关键参数。为了实现最佳的流变性能,研究人员通过调控原材料之间不同的比例,达到最优的结构效果。图2a的结果表明,二氧化硅粒子的加入,可增强树脂的混溶性。研究人员还测试了材料的流变性质,如图2b-d所示,油墨表现出剪切变稀行为,其中其粘度随着剪切速率的增加而降低。通过进一步的比例调控和测试,研究人员所制备的材料具有与人类心脏组织(E=29-41kPa)相当的超低有效机械模量(E=29±12kPa),可实现对组织施加最小应力的方式在心外膜表面上轻轻地连接。此外,通过循环测试和滞后测试,该材料表现出良好的稳定性和较小的滞后性。
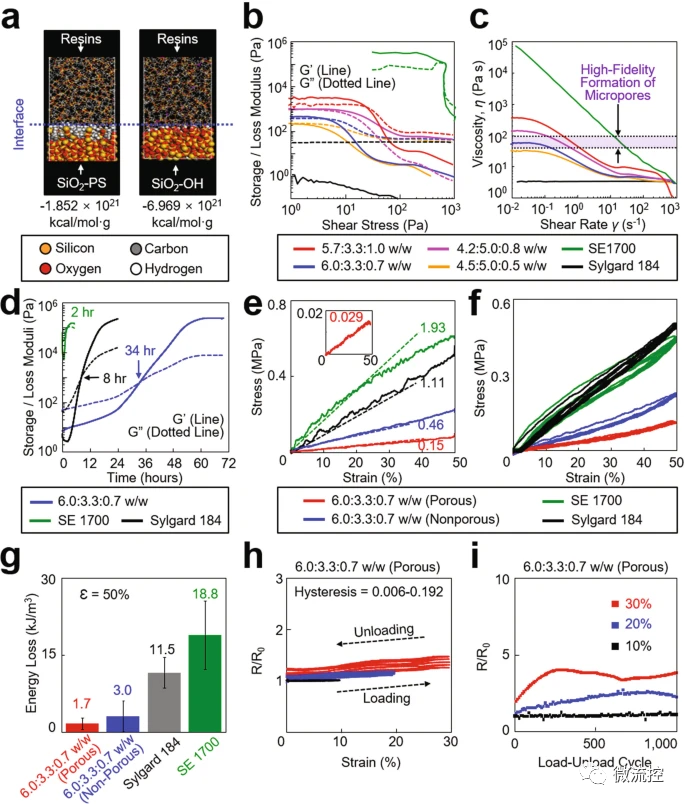
图2 多孔柔性生物传感器材料结构-性能关系
此外,研究人员所制备的多孔柔性生物传感器可根据不同动物的心脏进行定制打印(图3a),通过对比可以看出(图3b),该打印设备具有较宽的打印空间分辨率。此外,在该研究中,双极性记录配置不仅用于降低共模噪声(如电力线干扰),还用于抑制串扰以高保真度记录心电图(ECG)信号。
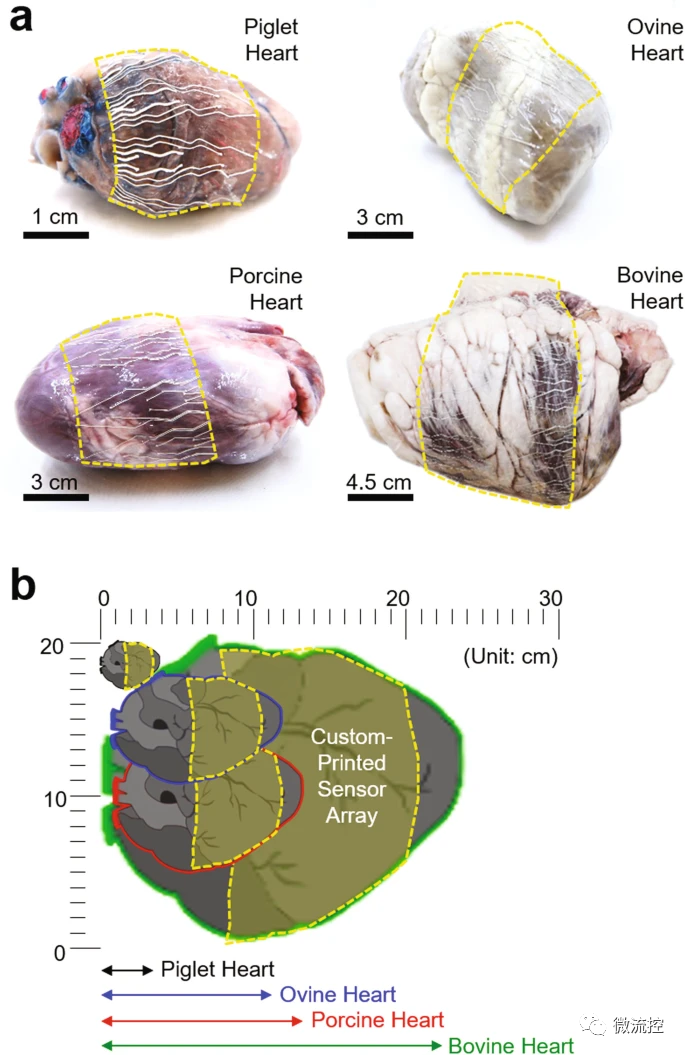
图3 快速定制打印多孔柔性生物传感器
进一步地,研究人员评估了定制打印器件在体内健康小鼠(n=5)和猪心脏(n=2)中心外膜心电图(ECG)的时空记录中的能力。在应用温盐水溶液溶解薄膜后,将器件(50μm厚)通过毛细管粘附力紧密粘附在心外膜表面(图4a)。图4b显示了时空记录的小鼠(左图)和猪(右图)心电信号的后处理3D数据的相应测量结果。应变不敏感的多孔弹性行为(即,在循环负载下可忽略不计的电滞后,应变为<30%)及其在跳动的心外膜表面上的稳态接触使得心外ECG信号的高保真度采集不会随时间推移而明显降低信号质量(图4c)。
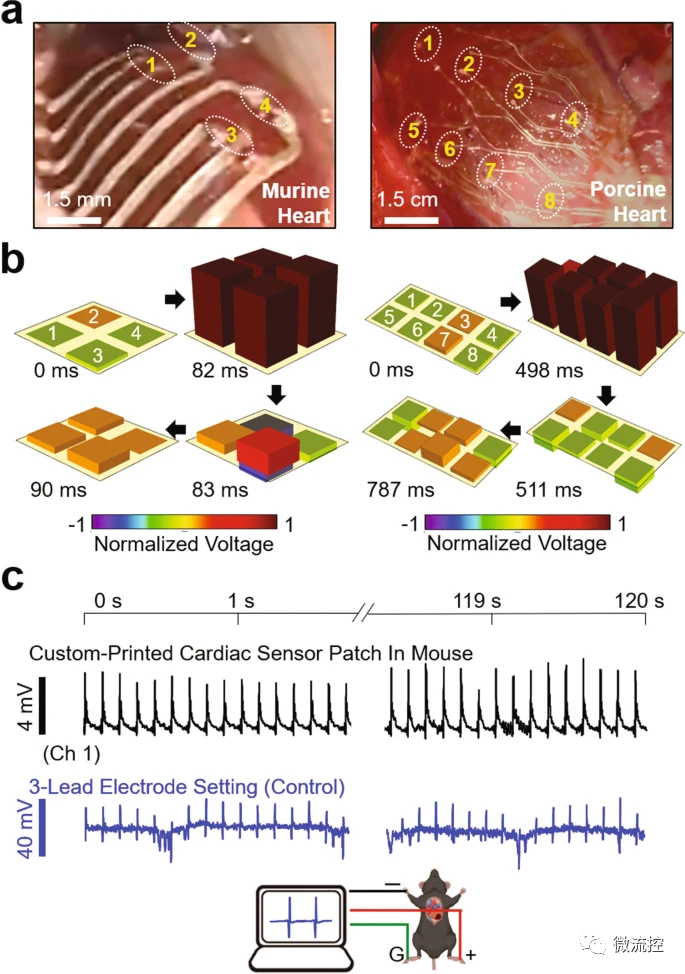
图4 定制柔性传感器用于体内心外膜心电图信号的时空记录
术中心外膜测绘有助于定位病理生理疾病起源的关键区域,例如急性心肌梗死后心律失常,从而为指导手术治疗提供重要信息,特别是当需要确定梗死边界时。为了证明定制打印器件在这种手术环境中的效用,研究人员在体内小鼠急性心肌梗死模型中对心外ECG信号进行了术中时空映射。成年小鼠接受左开胸术以暴露心脏的腹侧部分,然后在心外膜表面上放置定制打印的传感器阵列(共六个双极记录通道)以覆盖心室性心痺(图5a)。永久固定左冠状动脉的手术按照先前研究中报告的相同程序进行。心外膜心电图测量的代表性结果如图5b所示。图5c显示了使用三导联电极组同时获得的控制测量结果,显示了倒易的ST段凹陷以确认缺血事件的发生。上述结果表明,该器件与心外膜表面保持了紧密的耦合,在整个记录期间(30min超10000次跳动)没有改变位置。
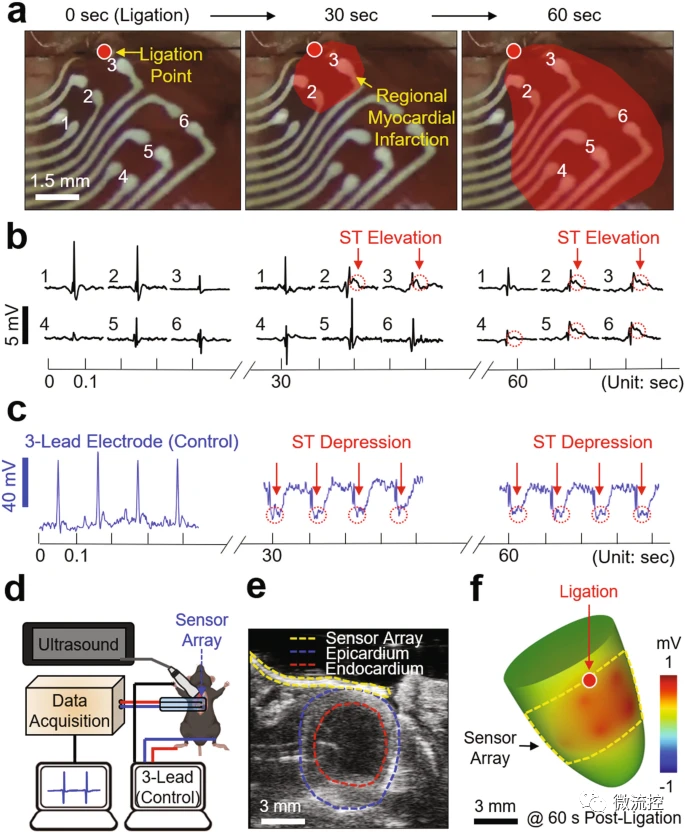
图5 柔性传感器用于小鼠心肌梗死模型的术中心外膜标测
由于开放式网格布局和薄膜设计(50μm厚),器件的半透明性使同时超声成像成为可能,作为实时验证心肌梗死区域的位置和大小的手段。图5d为实验装置,图5e显示了具有代表性的短轴超声图像,清楚地可视化了装置(黄色圆圈)以及心脏的上睑(蓝色圆圈)和心内膜(红色圆圈)。图5f显示了从超声图像和连接60秒后时空记录的ECG信号重建的后处理3D图像。这些结果证实,随着器件厚度的减小,成像伪影(例如,记录电极对的阴影)被最小化。
最后,研究人员对器件的生物相容性,抗生物污染能力和对心脏功能的影响进行了系统的评估。
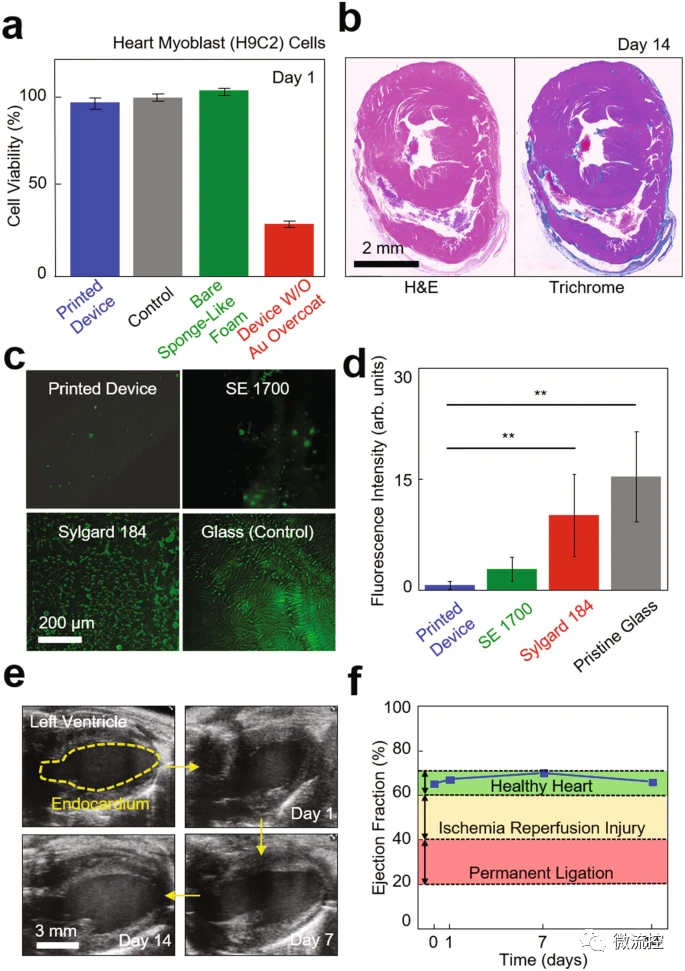
图6 柔性传感器生物相容性、抗生物污染和对心脏功能的影响
论文链接:
https://doi.org/10.1038/s41467-021-23959-3
延伸阅读:
《印刷和柔性传感器技术及市场-2021版》
《医疗柔性电子技术及市场趋势-2020版》
《即时诊断应用的生物传感器技术及市场-2022版》
